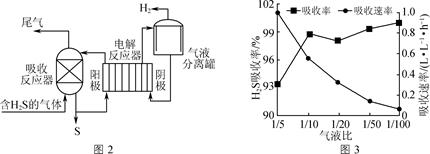
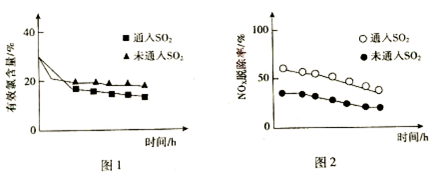
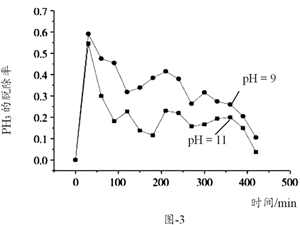
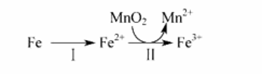甲醇水蒸气重整制氢 (SRM) 系统简单,产物中 H 2 含量高、 CO 含量低 (CO 会损坏燃料电池的交换膜 ) ,是电动汽车氢氧燃料电池理想的氢源。反应如下 :
反应 Ⅰ ( 主 ) :CH 3 OH(g)+ H 2 O(g) ![]() CO 2 (g)+ 3H 2 (g) ΔH 1 =+49kJ/mol
CO 2 (g)+ 3H 2 (g) ΔH 1 =+49kJ/mol
反应 Ⅱ ( 副 ) :H 2 (g)+ CO 2 (g) ![]() CO(g)+ H 2 O(g) ΔH 2 =+41kJ/mol
CO(g)+ H 2 O(g) ΔH 2 =+41kJ/mol
温度高于 300 ℃则会同时发生反应Ⅲ : CH 3 OH(g) ![]() CO(g)+2H 2 (g) ΔH 3
CO(g)+2H 2 (g) ΔH 3
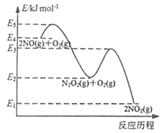
( 1 )计算反应 Ⅲ的 ΔH 3 = _________ 。
( 2 )反应 1 能够自发进行的原因是 _______________ ,升温有利于提高 CH 3 OH 转化率,但也存在一个明显的缺点是 __________ 。
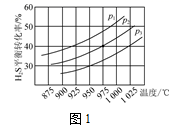
( 3 )右图为某催化剂条件下, CH 3 OH 转化率、 CO 生成率与温度的变化关系。
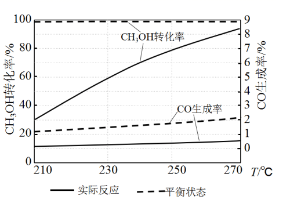
①随着温度的升高 ,CO 的实际反应生成率没有不断接近平衡状态生成率的原因是 ____________ ( 填标号 ) 。
A. 反应 Ⅱ逆向移动
B. 部分 CO 转化为 CH 3 OH
C. 催化剂对反应 Ⅱ的选择性低
D. 催化剂对反应 Ⅲ的选择性低
②随着温度的升高, CH 3 OH 实际反应转化率不断接近平衡状态转化率的原因是 ______ 。
③写出一条能提高 CH 3 OH 转化率而降低 CO 生成率的措施 _________ 。
( 4 ) 250 ℃,一定压强和催化剂条件下, 1.00molCH 3 OH 和 1.32molH 2 O 充分反应 ( 已知此条件下可忽略反应 Ⅲ ), 平衡时测得 H 2 为 2.70mol,CO 有 0.030mol, 试求反应 Ⅰ中 CH 3 OH 的转化率 _________ ,反应 Ⅱ的平衡常数 _________ ( 结果保留两位有效数字 )
答案
+90kJ/mol 反应 Ⅰ为熵增加的反应 CO 含量升高,破坏燃料电池的交换膜 C 升温反应速率加快 其它条件不变,提高 n( 水 )/n( 甲醇 ) 的比例 ( 或其它条件不变,选择更合适的借化剂 ) 91% 5.6×10 -3
【详解】
( 1 )反应 Ⅰ加上反应Ⅱ得到: CH 3 OH(g) ![]() CO(g)+2H 2 (g) ΔH 3 = +90kJ/mol 。
CO(g)+2H 2 (g) ΔH 3 = +90kJ/mol 。
( 2 )反应自发进行的要求是 △ G= △ H - T △ s < 0 ,此反应的 △ H > 0 ,所以反应自发进行的原因就是 △ s > 0 ,即反应为熵增反应。升温会促进反应 Ⅲ的发生,提高 CO 的含量,而 CO 会破坏该电池的交换膜。
( 3 ) ①工业生产中,一般不会等待反应达到平衡后再进行下一道工序,多数都是进行一段时间的反应就将体系取出,所以一般来说,反应的速度越快,取出的体系就越接近应该达到的平衡态。随着反应温度的升高,速度加快,但是 CO 的生产率并没有接近反应的平衡态,说明该反应使用的催化剂对于反应 Ⅱ几乎没有加速作用,所以选项 C 正确,选项 D 错误。三个反应都吸热,所以升温都正向移动,不会促进 CO 转化为甲醇,选项 A 、选项 B 都错误。
②由①的叙述可以得到答案为:升温反应速率加快。
③加入水蒸气,可以调高甲醇的转化率,同时使反应Ⅱ的平衡向逆反应方向移动,从而降低了 CO 的生成率。加入更合适的催化剂,最好只催化反应 Ⅰ,不催化反应Ⅱ,这样也能达到目的。
( 4 )达平衡时 CO 有 0.03mol ,根据反应 Ⅱ得到参与反应的氢气为 0.03mol ,所以反应 Ⅰ生成的氢气为 2.73mol (平衡剩余氢气 2.7mol ),根据反应 Ⅰ,消耗的甲醇为 0.91mol ,所以甲醇转化率为 91% 。根据反应 Ⅰ的数据,消耗的水为 0.91mol ,生成的 CO 2 为 0.91mol ,则剩余 1.32-0.91=0.41mol 水,在反应 Ⅱ中应该消耗 0.03molCO 2 ,生成 0.03molCO 和 0.03mol 水,所以达平衡时,水为 0.41+0.03=0.44mol , CO 2 为 0.91-0.03=0.88mol 。所以反应 Ⅱ的平衡常数为(设容器体积为 V ) 。