福建多个科研机构经过长期联合研究发现,使用 和改性的
基催化剂,可打通从合成气经草酸二甲酯常压催化加氢制备乙二醇的技术难关。下列说法正确的是
A .草酸属于无机物 B . 与石墨互为同分异构体
C . 属于过渡元素 D .催化剂通过降低焓变加快反应速率
C
【详解】 A .草酸属于二元弱酸,即乙二酸,属于有机物, A 错误;
B . C 60 与石墨是碳元素的不同单质,互为同素异形体, B 错误;
C . Cu 为 ⅠB 族,属于过渡元素, C 正确;
D .催化剂通过降低反应的活化能加快反应速率,反应焓变不变, D 错误;
故选 C 。
某兴趣小组设计实验探究 ,催化空气氧化
的效率。回答下列问题:
步骤 Ⅰ 制备
在通风橱中用下图装置制备 ( 加热及夹持装置省略 ) ,反应方程式:
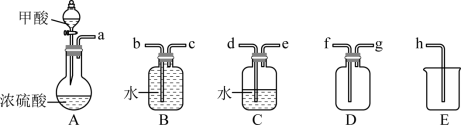
(1) 装置 A 中盛放甲酸的仪器的名称是 。
(2) 从 B 、 C 、 D 中选择合适的装置收集 ,正确的接口连接顺序为 a→_______→_______→_______→_______→h( 每空填一个接口标号 ) 。
步骤 Ⅱ 检验
将 通入新制银氨溶液中,有黑色沉淀生成。
(3) 该反应的化学方程式为 。
步骤 Ⅲ 探究 催化空气氧化
的效率
将一定量 与空气混合,得到
体积分数为 1% 的气体样品。使用下图装置 ( 部分加热及夹持装置省略 ) ,调节管式炉温度至
,按一定流速通入气体样品。 ( 已知:
是白色固体,易吸水潮解:
)
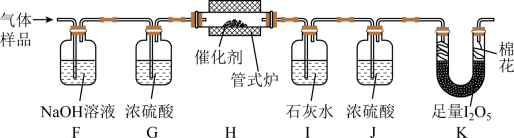
(4) 通入 ( 已折算为标况 ) 的气体样品后,继续向装置内通入一段时间氮气,最终测得 U 形管内生成了
。
① 能证明 被空气氧化的现象是 ;
② 被催化氧化的百分率为 ;
③ 若未通入氮气, ② 的结果将 ( 填 “ 偏大 ”“ 偏小 ” 或 “ 无影响 ”) 。
(5) 探究气体与催化剂接触时长对催化氧化效率的影响时,采用 方法可以缩短接触时长。
(6) 步骤 Ⅲ 装置存在的不足之处是 。
(1) 分液漏斗
(2)a→d→e→c→b
(3)
(4) 石灰水变浑浊 60% 偏大
(5) 增大气体样品流速
(6) 尾气出口未加防潮装置 ( 或其他相似表述 )
【分析】在通风橱中用下图装置制备一氧化碳,用 A 装置制取一氧化碳,该气体中含有甲酸蒸气,故用水除去甲酸,再用 B 装置排水收集一氧化碳气体,排出的水用 E 中的烧杯接收。根据气体样品通过氢氧化钠吸收空气中的二氧化碳,浓硫酸吸水,一氧化碳在 H 中被氧气氧化生成二氧化碳,二氧化碳能被石灰水吸收, J 中的浓硫酸吸收气体中的水蒸气,干燥的一氧化碳和 ,进而测定生成的碘的质量,计算一氧化碳的被氧化的百分率。据此解答。
【详解】( 1 )装置 A 中盛放甲酸的仪器为分液漏斗。
( 2 )用 C 除去甲酸, B 收集一氧化碳, E 接收排出的水,故接口连接顺序为 a→d→e→c→b→h 。
( 3 )一氧化碳和银氨溶液反应生成黑色的银,同时生成碳酸铵和氨气,方程式为: 。
( 4 )一氧化碳被氧气氧化生成二氧化碳,能使澄清的石灰水变浑浊。碘的物质的量为 ,则结合方程式分析,还有 0.002mol 一氧化碳未被氧气氧化, 11.2L 气体为 0.5mol 其中一氧化碳为 0.005mol ,则被氧化的一氧化碳为 0.005-0.002=0.003mol ,则被氧化的百分率为
。如果没有通入氮气则计算的未被氧化的一氧化碳的物质的量减少,则被氧化的百分率增大。
( 5 )增大气流速率可以提高催化效率。
( 6 ): 是白色固体,易吸水潮解,但该装置出气口未加防潮装置。
氨是水体污染物的主要成分之一,工业上可用次氯酸盐作处理剂,有关反应可表示为:
①
②
在一定条件下模拟处理氨氮废水:将 的氨水分别和不同量的
混合,测得溶液中氨去除率、总氮 ( 氨氮和硝氮的总和 ) 残余率与
投入量 ( 用 x 表示 ) 的关系如下图所示。下列说法正确的是
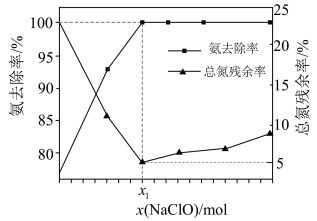
A . 的数值为 0.009
B . 时,
C . 时, x 越大,生成
的量越少
D . 时,
C
【详解】 A . x 1 时,氨的去除率为 100% 、总氮残留率为 5 ,
, 95% 的氨气参与反应 ① 、有 5% 的氨气参与反应 ② ,反应 ① 消耗
,参与反应 ② 消耗
,
, A 错误;
B . x>x 1 时,反应 ① 也生成氯离子,所以 , B 错误;
C . x>x 1 时, x 越大,氨总去除率不变,氮残余率增大,说明生成的硝酸根离子越多,生成 N 2 的量越少, C 正确;
D . x=x 1 时,氨的去除率为 100% ,溶液中没有 和 ClO - ,含有 Na + 、 H + 、
、 Cl - 和 OH - ,根据电荷守恒得
, D 错误;
故本题选 C 。
粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰为原料 ( 主要含 和
等 ) 提铝的工艺流程如下:
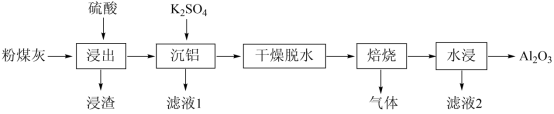
回答下列问题:
(1)“ 浸出 ” 时适当升温的主要目的是 , 发生反应的离子方程式为 。
(2)“ 浸渣 ” 的主要成分除残余 外,还有 。实验测得,
粉煤灰 (
的质量分数为
) 经浸出、干燥后得到
“ 浸渣 ”(
的质量分数为
) ,
的浸出率为 。
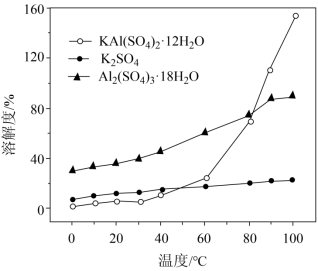
(3)“ 沉铝 ” 时,体系中三种物质的溶解度曲线如下图所示,加入 沉铝的目的是 , “ 沉铝 ” 的最佳方案为 。
(4)“ 焙烧 ” 时,主要反应的化学方程式为 。
(5)“ 水浸 ” 后得到的 “ 滤液 2” 可返回 工序循环使用。
(1) 提高浸出率 ( 或提高浸出速率 )
(2) 和
84%
(3) 使更多的铝元素转化为晶体析出,同时保证晶体纯度 高温溶解再冷却结晶
(4) 或
(5) 沉铝
【分析】粉煤灰为原料 ( 主要含 SiO 2 、 Al 2 O 3 和 CaO 等 ) 加入硫酸,浸渣为二氧化硅、硫酸钙,加入硫酸钾,产生复盐明矾沉铝,干燥脱水,焙烧产生氧化铝、硫酸钾和二氧化硫或三氧化硫气体,水浸除去硫酸钾,得到氧化铝。
【详解】( 1 )温度高速率大, “ 浸出 ” 时适当升温的主要目的是提高反应速率,提高浸出率; Al 2 O 3 和 H 2 SO 4 发生反应生成 Al 2 (SO 4 ) 3 和 H 2 O ,离子反应方程式为 Al 2 O 3 +6H + =2Al 3+ +3H 2 O ;
故答案为:提高浸出率 ( 或提高浸出速率 ) ; Al 2 O 3 +6H + =2Al 3+ +3H 2 O 。
( 2 ) “ 浸渣 ” 的主要成分除残余 Al 2 O 3 外,还有二氧化硅、硫酸钙; 5.0g 粉煤灰 Al 2 O 3 的质量为 5.0g×30%=1.5g , 3.0g“ 浸渣 ”Al 2 O 3 的质量为 3.0g×8%=0.24g ,则 Al 2 O 3 的浸出率为 ;
故答案为: SiO 2 和 CaSO 4 ; 84% 。
( 3 )根据沉铝体系中, Al 2 (SO 4 ) 3 ·18H 2 O 溶解度最大, KAl(SO 4 ) 2 ·12H 2 O 溶解度最小,更容易析出,加入 K 2 SO 4 沉铝的目的是更多的使 Al 2 (SO 4 ) 3 转化为 KAl(SO 4 ) 2 ·12H 2 O ,使更多的铝元素转化为晶体析出,同时保证晶体纯度; KAl(SO 4 ) 2 ·12H 2 O 溶解度受温度影响较大, “ 沉铝 ” 的最佳方案为高温溶解再冷却结晶;
故答案为:使更多的铝元素转化为晶体析出,同时保证晶体纯度;高温溶解再冷却结晶。
( 4 ) “ 焙烧 ” 时, KAl(SO 4 ) 2 分解为 K 2 SO 4 、 Al 2 O 3 和 SO 3 或 K 2 SO 4 、 Al 2 O 3 、 SO 2 和 O 2 ,反应方程式为 2KAl(SO 4 ) 2 K 2 SO 4 +Al 2 O 3 +3SO 3 ↑ 或 4KAl(SO 4 ) 2
2K 2 SO 4 +2Al 2 O 3 +6SO 2 ↑+3O 2 ↑ ;
故答案为: 2KAl(SO 4 ) 2 K 2 SO 4 +Al 2 O 3 +3SO 3 ↑ 或 4KAl(SO 4 ) 2
2K 2 SO 4 +2Al 2 O 3 +6SO 2 ↑+3O 2 ↑ 。
( 5 ) “ 水浸 ” 后得到的 “ 滤液 2” 成分为 K 2 SO 4 ,可在沉铝工序循环使用;
故答案为:沉铝。
异丙醇 可由生物质转化得到,催化异丙醇脱水制取高值化学品丙烯
的工业化技术已引起人们的关注,其主要反应如下:
Ⅰ.
Ⅱ.
回答下列问题:
(1) 已知 ,则
燃烧生成
和
的热化学方程式为 。
(2) 在 下,刚性密闭容器中的反应体系内水蒸气浓度与反应时间关系如下表:
| 反应时间 | 0 | 4 | 8 | 12 | t | 20 |
| | 0 | 2440 | 3200 | 3600 | 4000 | 4100 |
① 内,
;
②t 16( 填 “>”“<” 或 “=”) 。
(3) 在恒温刚性密闭容器中,反应 Ⅰ 、 Ⅱ 均达到平衡的判据是 ( 填标号 ) 。
a. 的分压不变 b. 混合气体密度不变
c. d.
(4) 在一定条件下,若反应 Ⅰ 、 Ⅱ 的转化率分别为 98% 和 40% ,则丙烯的产率为 。
(5) 下图为反应 Ⅰ 、 Ⅱ 达到平衡时 与温度的关系曲线。
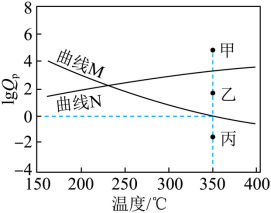
( 已知:对于可逆反应 ,任意时刻
,式中
) 表示物质 × 的分压 )
① 在 恒压平衡体系中充入少量水蒸气时,反应 Ⅰ 的的状态最有可能对应图中的 点 ( 填 “ 甲 ”“ 乙 ” 或 “ 丙 ”) ,判断依据是 。
② 时,在密闭容器中加入一定量的
,体系达到平衡后,测得
的分压为
,则水蒸气的分压为
( 用含 x 的代数式表示 ) 。
(1)
(2) 190 >
(3)ad
(4)58.8%
(5) 甲 反应 I 平衡曲线为 N ,恒压时充入水蒸气,
【详解】( 1 )设 Ⅲ ,根据盖斯定律 Ⅲ-2×Ⅰ 得
。
( 2 ) ① 内,
,则
;
② 、
、
, △ c (H 2 O) 逐渐减小,说明反应速率减小,
内, Δ c (H 2 O)=400ppm ,
内, Δ c (H 2 O)=400ppm ,则 t-12>4 ,即 t>16 。
( 3 ) a . H 2 O 的分压不变,则 C 3 H 6 的分压也不变,反应 1 、 Ⅱ 各组分分压不变,反应 1 、 Ⅱ 均达到平衡, a 正确;
b .反应物和生成物均为气体,混合气体的总质量不变,刚性密闭容器体积不变,则混合气体密度不变,不能作为反应 I 、 Ⅱ 均达到平衡的判据, b 错误;
c .当 时,反应不一定达到平衡,不能作为反应 1 、 Ⅱ 均达到平衡的判据, c 错误;
d . ,说明正逆反应速率相等,反应 I 达平衡,各组分分压不变, C 3 H 6 的分压不变,说明反应 Ⅱ 也达平衡, d 正确;
故选 ad 。
( 4 )设 C 3 H 8 O 的物质的量为 1mol ,若 lmol C 3 H 8 O 完全反应,理论上生成 1mol C 3 H 6 ,因为反应 Ⅰ 、 Ⅱ 的转化率分别为 98% 和 40% ,反应 I 生成 1mol×98%=0.98mol C 3 H 6 ,反应 Ⅱ 消耗了 40% C 3 H 6 ,则达平衡时 C 3 H 6 的物质的量为 0.98mol×(1-40%)=0.588mol ,所以丙烯的产率为 =58.8% 。
( 5 ) ① 反应 I 为气体体积增大的吸热反应,反应 Ⅱ 为气体体积减小的放热反应,则升高温度,反应 I 正向移动, 逐渐增大,反应 Ⅱ 逆向移动,
逐渐减小,即反应 I 为平衡曲线为 N ,反应 Ⅱ 平衡曲线为 M ;在 350℃ 恒压平衡体系中充入少量水蒸气时,对于反应 I 而言,相当于增大生成物浓度,使得
>
,即 lg
增大,反应 I 的状态最有可能对应图中的甲;
② 由图可知, 350°C 时达平衡后, =0 ,则 350℃ 时
=
=1 ,设水蒸气的平衡分压为 a MPa ,则反应 II 的 C 3 H 6 起始分压为 a MPa ,对反应 Ⅱ 列三段式有
,解得 a=
MPa 。
1962 年首个稀有气体化合物 问世,目前已知的稀有气体化合物中,含氙 ( 54 Xe) 的最多,氪 ( 36 Kr) 次之,氩 ( 18 Ar) 化合物极少。
是
与
分子形成的加合物,其晶胞如下图所示。
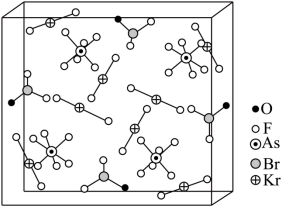
回答下列问题:
(1) 基态 原子的价电子排布式为 。
(2) 原子的活泼性依序增强,原因是 。
(3) 晶体熔点:
( 填 “>”“<” 或 “=”) ,判断依据是 。
(4) 的中心原子
的杂化轨道类型为 。
(5) 加合物中
,晶体中的微粒间作用力有 ( 填标号 ) 。
a. 氢键 b. 离子键 c. 极性共价键 d. 非极性共价键
(1)
(2) 同族元素,从上而下原子半径逐渐增大,原子核对外层电子的有效吸引逐渐减弱,失电子能力逐渐增强
(3) < 二者为同构型的分子晶体, 相对分子质量大,范德华力大,熔点高
(4)
(5) 2 bc
【详解】( 1 ) 位于元素周期表中第四周期 VA 族,原子序数为 33 ,由构造原理写出其价电子排布式为
。
( 2 )同族元素,从上而下原子半径逐渐增大,原子核对外层电子的有效吸引逐渐减弱,失电子能力逐渐增强,故 原子的活泼性依序增强。
( 3 ) 和
是同构型的分子晶体,
相对分子质量大,范德华力大,熔点高,晶体熔点:
<
。
( 4 ) 的中心原子
的价层电子对数为: 3+
=4 ,杂化轨道类型为
。
( 5 )由晶胞结构可知,其中含有 8 个 、 4 个
、 4 个
,则
加合物中
2 ,晶体中的微粒间作用力有离子键、极性共价键,故选 bc 。
实验室需对少量污染物进行处理。以下处理方法和对应的反应方程式 均错误 的是
A .用硫磺处理洒落在地上的水银:
B .用盐酸处理银镜反应后试管内壁的金属银:
C .用烧碱溶液吸收蔗糖与浓硫酸反应产生的刺激性气体:
D .用烧碱溶液吸收电解饱和食盐水时阳极产生的气体:
B
【详解】 A . S 和 Hg 发生化合反应生成 HgS ,可以用硫磺处理洒落在地上的水银,方程式为: ,处理方法和对应的反应方程式正确,不合题意;
B . Ag 不活泼,不能和盐酸反应生成氢气,处理方法和对应的反应方程式均错误,符合题意;
C .蔗糖与浓硫酸反应产生的刺激性气体为 SO 2 ,可以用 NaOH 溶液吸收 SO 2 ,离子方程式为: ,处理方法和对应的反应方程式均正确,不符合题意;
D .电解饱和食盐水时阳极产生的气体为 Cl 2 ,可以用 NaOH 溶液吸收 Cl 2 ,离子方程式为: ,处理方法和对应的反应方程式均正确,不符合题意;
故选 B 。
一种化学 “ 自充电 ” 的锌 - 有机物电池,电解质为 和
水溶液。将电池暴露于空气中,某电极无需外接电源即能实现化学自充电,该电极充放电原理如下图所示。下列说法正确的是
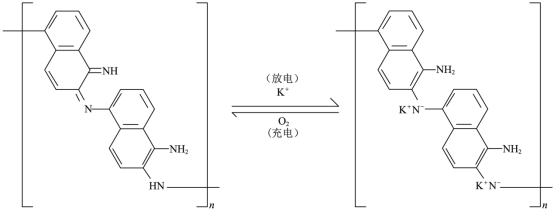
A .化学自充电时, 增大
B .化学自充电时,电能转化为化学能
C .化学自充电时,锌电极反应式:
D .放电时,外电路通过 电子,正极材料损耗
A
【详解】 A .由图可知,化学自充电时,消耗 O 2 ,该反应为 O 2 +2H 2 O+4e - =4OH - , 增大,故 A 正确;
B .化学自充电时,无需外接电源即能实现化学自充电,该过程不是电能转化为化学能,故 B 错误;
C .由图可知,化学自充电时,锌电极作阴极,该电极的电极反应式为 O 2 +2H 2 O+4e - =4OH - ,故 C 错误;
D .放电时, 1mol 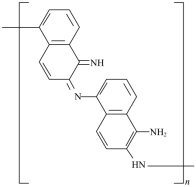 转化为
转化为 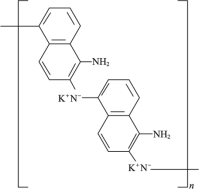 ,消耗 2mol K + ,外电路通过
,消耗 2mol K + ,外电路通过 电子时,正极物质增加 0.02mol K + ,增加的质量为 0.02mol×39g/mol =0.78g ,故 D 错误;
故选 A 。
锂辉石是锂的重要来源,其焙烧后的酸性浸出液中含有 和
杂质离子,可在 0~14 范围内调节
对其净化 ( 即相关离子浓度
) 。
时,
与
关系见下图 ( 碱性过强时
和
会部分溶解 ) 。下列说法正确的是
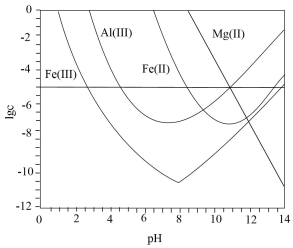
A . 可被净化的
区间最大
B .加入适量 ,可进一步提升净化程度
C .净化的先后顺序:
D .
B
【详解】 A .对离子净化时,相关离子浓度 c <10 -5 mol/L ,则 lg c <-5 ,由图可知,可作净化的 pH 区间最大的是 Fe 3+ , A 错误;
B .加入适量 H 2 O 2 ,可将 Fe 2+ 氧化为 Fe 3+ ,提高净化程度, B 正确;
C .由图可知,净化的先后顺序为 , C 错误;
D .对离子净化时,相关离子浓度 c <10 -5 mol/L , lg c <-5 ,,由图可知, Fe 3+ 完全沉淀的 pH 约为 2.5 , c (H + )=10 -2.5 mol/L , c (OH - )=10 -11.5 mol/L , , Al 3+ 完全沉淀的 pH 约为 4.5 , c (H + )=10 -4.5 mol/L , c (OH - )=10 -9.5 mol/L ,
, Fe 2+ 完全沉淀的 pH 约为 8.5 , c (H + )=10 -8.5 mol/L , c (OH - )=10 -5.5 mol/L ,
,则有
, D 错误;
故选 B 。
用铬铁合金 ( 含少量 单质 ) 生产硫酸铬的工艺流程如下:
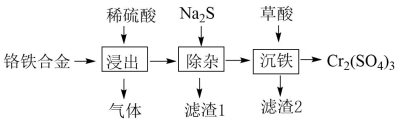
下列说法 错误 的是
A . “ 浸出 ” 产生的气体含有 B . “ 除杂 ” 的目的是除去
元素
C .流程中未产生六价铬化合物 D . “ 滤渣 2” 的主要成分是
D
【分析】由流程可知,加入稀硫酸溶解,生成气体为氢气,溶液中含 加入 Na 2 S 分离出滤渣 1 含 CoS 和 NiS ,
不会沉淀,再加入草酸除铁生成 FeC 2 O 4 ,过滤分离出硫酸铬,以此来解答。
【详解】 A .四种金属均与稀硫酸反应生成 H 2 , A 正确;
B .共有四种金属,由流程可知,沉铁后分离出硫酸铬,则 “ 除杂 " 的目的是除去 Ni 、 Co 元素, B 正确;
C .由上述分析可知,流程中未产生六价铬化合物, C 正确;
D . “ 滤渣 2” 的主要成分是 FeC 2 O 4 , D 错误;
故本题选 D 。
探究醋酸浓度与电离度 关系的步骤如下,与相关步骤对应的操作或叙述正确的
| | 步骤 | 操作或叙述 |
| A | Ⅰ. 用 | 滴定时应始终注视滴定管中的液面 |
| B | Ⅱ. 用标定后的溶液配制不同浓度的醋酸溶液 | 应使用干燥的容量瓶 |
| C | Ⅲ. 测定步骤 Ⅱ 中所得溶液的 | 应在相同温度下测定 |
| D | Ⅳ. 计算不同浓度溶液中醋酸的电离度 | 计算式为 |
A . A B . B C . C D . D
C
【详解】 A .中和滴定时眼睛应始终注视锥形瓶内溶液颜色的变化, A 错误;
B .配制不同浓度的醋酸溶液时,容量瓶不需要干燥, B 错误;
C .温度影响醋酸的电离平衡,因此测定步骤 Ⅰ 中所得溶液的 时应在相同温度下测定, C 正确;
D .电离度是指弱电解质在溶液里达电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的)的百分数,因此醋酸的电离度计算式为 , D 错误;
答案选 C 。
某非线性光学晶体由钾元素 (K) 和原子序数依次增大的 X 、 Y 、 Z 、 W 四种短周期元素组成。 X 与 Y 、 Z 与 W 均为同周期相邻元素, X 的核外电子总数为最外层电子数的 2 倍, Z 为地壳中含量最多的元素。下列说法正确的是
A .简单氢化物沸点: B .
分子的空间构型为三角锥形
C .原子半径: D .最高价氧化物对应水化物的碱性:
A
【分析】 X 的核外电子总数为最外层电子数的 2 倍, X 为 Be ; Z 为地壳中含量最多的元素, Z 为 O , X 与 Y 、 Z 与 W 均为同周期相邻元素, Y 为 B , W 为 F ,据此解答。
【详解】 A . 常温下为液态, HF 常温下为气体,沸点
,故 A 正确;
B . 为 BF 3 ,中心 B 原子有 3 对价电子且没有孤电子对,空间构型为平面三角形,故 B 错误;
C .四种元素为同周期元素,随核电荷数增大原子半径减小,原子半径: Be>B>O>F ,故 C 错误;
D . Be 最高价氧化物水化物为 Be(OH) 2 ,溶液显两性, B 最高价氧化物的水化物为 H 3 BO 3 ,溶液显酸性,故 D 错误;
故选: A 。
常温常压下,电化学还原制氨气的总反应方程式: ,设
为阿伏加德罗常数的值,下列说法正确的是
A . 水中含有的孤电子对数为
B .每产生 失去的电子数为
C . 氨水中,含有的
分子数少于
D .消耗 ( 已折算为标况 ) 时,产生的
分子数为
D
【详解】 A . H 2 O 分子中孤电子对数为 =2 ,
H 2 O 的物质的量为
=0.5mol ,含有的孤电子对数为
,故 A 错误;
B .该反应中 N 2 中 N 元素化合价由 0 价下降到 -3 价, 34g 的物质的量为
=2mol ,每产生
,
得到 6mol 电子,数目为 6N A ,故 B 错误;
C .氨水的体积未知,无法计算 的分子数,故 C 错误;
D . 的物质的量为 0.5mol ,由方程式可知,消耗 0.5mol
,产生的 0.75mol
,数目为
,故 D 正确;
故选 D 。
络塞维是中药玫瑰红景天中含有的一种天然产物,分子结构见下图。关于该化合物下列说法正确的是
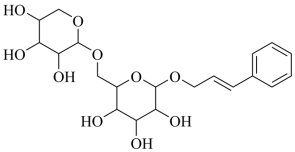
A .不能发生消去反应 B .能与醋酸发生酯化反应
C .所有原子都处于同一平面 D . 络塞维最多能与
反应
B
【详解】 A .该化合物的分子中,与羟基相连的碳原子的邻位碳原子上有氢原子,可发生消去反应, A 错误;
B .该化合物含有羟基,可与醋酸发生酯化反应, B 正确;
C .该化合物的结构中含有饱和碳原子,不可能所有原子处于同一平面上, C 错误;
D . 络塞维最多能与
反应,其中苯环消耗 3mol H 2 ,碳碳双键消耗 1mol H 2 , D 错误;
故选 B 。
3- 氧代异紫杉二酮是从台湾杉中提取的具有抗痛活性的天然产物。最近科学家完成了该物质的全合成,其关键中间体 (F) 的合成路线如下:
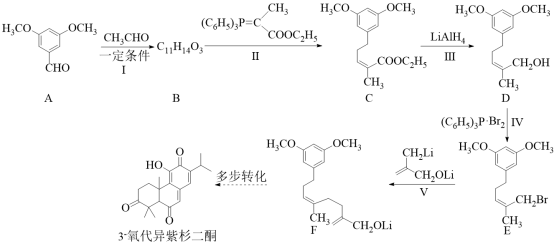
已知: 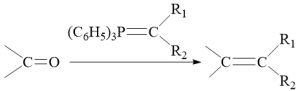
回答下列问题:
(1)A 的含氧官能团有醛基和 。
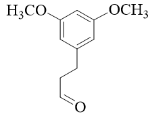
(2)B 的结构简式为 。
(3)Ⅳ 的反应类型为 ;由 D 转化为 E 不能使用 的原因是 。
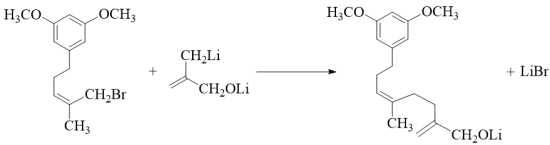
(4) 反应 Ⅴ 的化学方程式为 。
(5) 化合物 Y 是 A 的同分异构体,同时满足下述条件:
①Y 的核磁共振氢谱有 4 组峰,峰而积之比为 。
②Y 在稀硫酸条件下水解,其产物之一 ( 分子式为 ) 遇
溶液显紫色。则 Y 的结构简式为 。
(1) 醚键 ( 或醚基 )
(2) 
(3) 取代反应 会与碳碳双键发生加成反应 ( 或
会使醚键水解 )
(4) 
(5) 
【分析】有机合成可从正向和逆向共同进行推断,根据已知信息由 C 可推出 B 为 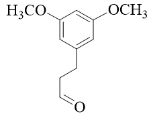 ,根据 C 到 D 的结构变化可知此步酯基发生水解反应,根据 D 到 E 的结构可知此步 Br 取代了羟基,根据 E 到 F 的结构可知脱去 LiBr ,为取代反应,据此进行推断。
,根据 C 到 D 的结构变化可知此步酯基发生水解反应,根据 D 到 E 的结构可知此步 Br 取代了羟基,根据 E 到 F 的结构可知脱去 LiBr ,为取代反应,据此进行推断。
【详解】( 1 ) A 的含氧官能团有醛基和醚键。
( 2 )根据分析可知, B 的结构简式为 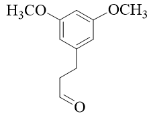 。
。
( 3 )反应 Ⅳ 中 Br 取代了羟基,为取代反应,此反应不用 HBr 的原因为 会与碳碳双键发生加成反应 ( 或
会使醚键水解 ) 。
( 4 )反应 Ⅴ 的化学方程式为  。
。
( 5 )产物之一 ( 分子式为 ) 遇
溶液显紫色,说明含有酚羟基,酚羟基是通过酯基水解得来的,又因为核磁共振氢谱有 4 组峰,峰而积之比为
,说明 Y 有两个甲基,综合可知 Y 的结构简式为
 。
。
劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
| 选项 | 劳动项目 | 化学知识 |
| A | 面包师用小苏打作发泡剂烘焙面包 | |
| B | 环保工程师用熟石灰处理酸性废水 | 熟石灰具有碱性 |
| C | 工人将模具干燥后再注入熔融钢水 | 铁与 |
| D | 技术人员开发高端耐腐蚀镀铝钢板 | 铝能形成致密氧化膜 |
A . A B . B C . C D . D
A
【详解】 A .小苏打是碳酸氢钠,不是碳酸钠,主要用来做膨松剂,故 A 符合题意;
B .熟石灰是氢氧化钙,具有碱性,可以用于处理酸性废水,故 B 不符合题意;
C .熔融的铁与水蒸气在高温下反应会生成四氧化三铁和氢气,因此必须将模具干燥,故 C 不符合题意;
D .钢板上镀铝,保护钢板,金属铝表面形成致密氧化膜而保护金属铝不被腐蚀,,故 D 不符合题意。
综上所述,答案为 A 。
甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是
| 甲 | | 乙 |
| 丙 | 丁 | 戊 |
A .原子半径:丁>戊>乙
B .非金属性:戊>丁>丙
C .甲的氢化物遇氯化氢一定有白烟产生
D .丙的最高价氧化物对应的水化物一定能与强碱反应
C
【分析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若是高氯酸,则戊为 Cl ,甲为 N 、乙为 F 、丙为 P 、丁为 S ,若是硫酸,则戊为 S ,甲为 C 、乙为 O 、丙为 Si 、丁为 P 。
【详解】 A .根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故 A 正确;
B .根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故 B 正确;
C .甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、乙烷等,则遇氯化氢不反应,没有白烟生成,故 C 错误;
D .丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,故 D 正确。
综上所述,答案为 C 。
实验室用 和浓盐酸反应生成
后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置 (“→” 表示气流方向 ) 不能达到实验目的的是
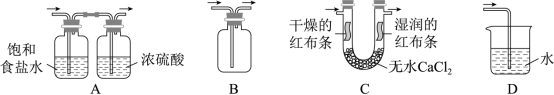
A . A B . B C . C D . D
D
【详解】 A .浓盐酸易挥发,制备的氯气中含有 HCl ,可用饱和食盐水除去 HCl , Cl 2 可用浓硫酸干燥, A 装置能达到实验目的,故 A 不符合题意;
B .氯气的密度大于空气,用向上排空气法收集, B 装置能收集氯气,故 B 不符合题意;
C .湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白性,故 C 不符合题意;
D .氯气在水中的溶解度较小,应用 NaOH 溶液吸收尾气, D 装置不能达到实验目的,故 D 符合题意;
答案选 D 。
我国科学家进行了如图所示的碳循环研究。下列说法正确的是
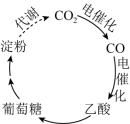
A .淀粉是多糖,在一定条件下能水解成葡萄糖
B .葡萄糖与果糖互为同分异构体,都属于烃类
C . 中含有
个电子
D . 被还原生成
A
【详解】 A .淀粉是由葡萄糖分子聚合而成的多糖,在一定条件下水解可得到葡萄糖,故 A 正确;
B .葡萄糖与果糖的分子式均为 C 6 H 12 O 6 ,结构不同,二者互为同分异构体,但含有 O 元素,不是烃类,属于烃的衍生物,故 B 错误;
C .一个 CO 分子含有 14 个电子,则 1molCO 中含有 14×6.02×10 23 =8.428×10 24 个电子,故 C 错误;
D .未指明气体处于标况下,不能用标况下的气体摩尔体积计算其物质的量,故 D 错误;
答案选 A 。
以熔融盐为电解液,以含 和
等的铝合金废料为阳极进行电解,实现
的再生。该过程中
A .阴极发生的反应为 B .阴极上
被氧化
C .在电解槽底部产生含 的阳极泥 D .阳极和阴极的质量变化相等
C
【分析】根据电解原理可知,电解池中阳极发生失电子的氧化反应,阴极发生得电子的还原反应,该题中以熔融盐为电解液,含 和
等的铝合金废料为阳极进行电解,通过控制一定的条件,从而可使阳极区 Mg 和 Al 发生失电子的氧化反应,分别生成 Mg 2+ 和 Al 3+ , Cu 和 Si 不参与反应,阴极区 Al 3+ 得电子生成 Al 单质,从而实现 Al 的再生,据此分析解答。
【详解】 A .阴极应该发生得电子的还原反应,实际上 Mg 在阳极失电子生成 Mg 2+ , A 错误;
B . Al 在阳极上被氧化生成 Al 3+ , B 错误;
C .阳极材料中 Cu 和 Si 不参与氧化反应,在电解槽底部可形成阳极泥, C 正确;
D .因为阳极除了铝参与电子转移,镁也参与了电子转移,且还会形成阳极泥,而阴极只有铝离子得电子生成铝单质,根据电子转移数守恒及元素守恒可知,阳极与阴极的质量变化不相等, D 错误;
故选 C 。
查看答案
单次付费有效 3.99 元
用于查看答案,单次有效 19.99元
包月VIP 9.99 元
用于查看答案,包月VIP无限次 49.99元