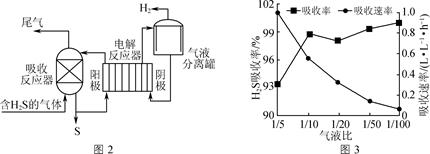
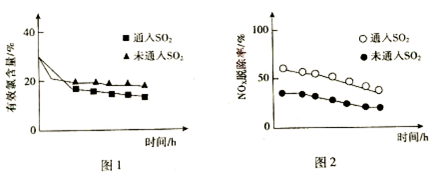
NaClO用途非常广泛。NaClO溶液中微粒的物质的量分布分数与溶液pH的关系如图-1所示,某NaClO溶液中有效氯含量与温度的关系如图-2所示。

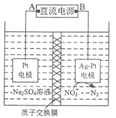
(1)工业上常用NaOH溶液与Cl2反应制备NaClO。Cl2与冷的NaOH溶液反应的离子方程式为____,当通入Cl2至溶液pH=5时,溶液中浓度最大的微粒是____(填“Cl2”“ClO-”或“HClO”)。
(2)NaClO溶液在空气中易失效,其与空气中CO2反应的化学方程式为____(已知H2CO3的Ka1、Ka2依次为4.47×10-7、4.68×10-11)。
(3)NaClO溶液可用于脱除黄磷生产尾气中PH3等有害气体。脱除PH3机理为:
H3O+ + ClO-= HClO + H2O
PH3 + HClO=![]()
![]() +ClO-= H3PO2 + Cl-
+ClO-= H3PO2 + Cl-
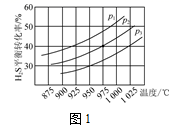
室温下,用3%的NaClO溶液分别在pH=9、pH=11时处理含PH3的尾气,PH3的脱除率如图-3所示:
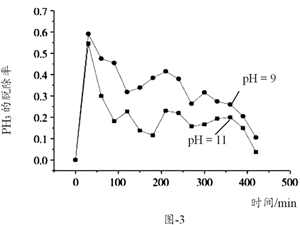
①下列措施能提高尾气中PH3的脱除率的是____(填标号)。
A.增大尾气的流速
B.将吸收液加热到40℃以上
C.采用气、液逆流的方式吸收尾气
D.吸收尾气的过程中定期补加适量NaClO并调节合适的溶液pH
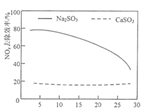
②已知PH3几乎不与NaOH溶液反应,黄磷生产尾气中除PH3外,还有大量的H2S等有害气体。黄磷尾气通过NaClO吸收液前需预先用30%NaOH溶液吸收处理,其目的是____。
③pH=9时PH3的脱除率总是比pH=11的大,其原因是____。
答案
Cl2 + 2OH-= Cl-+ ClO-+ H2O HClO NaClO + CO2 + H2O = NaHCO3 + HClO CD 吸收绝大多数H2S气体,减少NaClO的消耗量 pH=9时溶液中HClO的浓度较大,更有利于释放原子氧(氧化性较pH=11时强)
【分析】
(1) Cl2与冷的NaOH溶液反应生成NaClO和NaCl,结合图1分析解答;
(2)根据图1,pH=8时,溶液中HClO和ClO-的物质的量分布分数相等,即浓度相等,结合H2CO3的Ka1、Ka2分析判断HClO与H2CO3、HCO![]() 的酸性强弱,判断反应的产物;
的酸性强弱,判断反应的产物;
(3)①提高PH3的脱除率需要使反应充分进行,结合图2和PH3的脱除原理分析判断;②H2S等有害气体能够与氢氧化钠发生反应,也能NaClO吸收液发生氧化还原反应,而PH3几乎不与NaOH溶液反应,为了更好的除去PH3,需要减少NaClO的消耗,据此分析解答;③根据图3,结合PH3的脱除原理分析解答。
【详解】
(1)工业上常用NaOH溶液与Cl2反应制备NaClO,Cl2与冷的NaOH溶液反应生成NaClO和NaCl,反应的离子方程式为Cl2 + 2OH-= Cl-+ ClO-+ H2O;根据图1,当通入Cl2至溶液pH=5时,溶液中浓度最大的微粒是HClO,故答案为:Cl2 + 2OH-= Cl-+ ClO-+ H2O;HClO;
(2)NaClO易与空气中的CO2反应生成次氯酸,根据图1,pH=8左右时,溶液中HClO和ClO-的物质的量分布分数相等,即浓度相等,因此HClO的电离平衡常数K= c(H+)≈10-8,而H2CO3的Ka1、Ka2依次为4.47×10-7、4.68×10-11,所以酸性:H2CO3>HClO>HCO![]() ,因此反应的化学方程式为NaClO + CO2 + H2O = NaHCO3 + HClO,故答案为:NaClO + CO2 + H2O = NaHCO3 + HClO;
,因此反应的化学方程式为NaClO + CO2 + H2O = NaHCO3 + HClO,故答案为:NaClO + CO2 + H2O = NaHCO3 + HClO;
(3)①A.增大尾气的流速,反应不充分,PH3的脱除率会降低,故A不选;B.根据图2,温度越高,NaClO溶液中有效氯含量越低,将吸收液加热到40℃以上,NaClO溶液中有效氯含量较低,使得PH3的脱除率降低,故B不选;C.采用气、液逆流的方式吸收尾气,可以使气、液充分接触,反应更充分,PH3的脱除率提高,故C选;D.吸收尾气的过程中定期补加适量NaClO并调节合适的溶液pH,可以使尾气中PH3充分反应,提高PH3的脱除率,故D选;故答案为:CD;
②H2S等有害气体能够与氢氧化钠发生反应,也能NaClO吸收液发生氧化还原反应,而PH3几乎不与NaOH溶液反应,为了提高NaClO吸收液去除PH3的效率,因此黄磷尾气通过NaClO吸收液前预先用30%NaOH溶液吸收处理,减少NaClO的消耗量,故答案为:吸收绝大多数H2S气体,减少NaClO的消耗量;
③根据图3,pH=9时PH3的脱除率总是比pH=11的大,是因为pH=9时溶液中HClO的浓度较大,更有利于释放原子氧,故答案为:pH=9时溶液中HClO的浓度较大,更有利于释放原子氧。
【点睛】
本题的易错点和难点是(2),要注意判断NaClO与CO2反应的产物是碳酸钠还是碳酸氢钠。