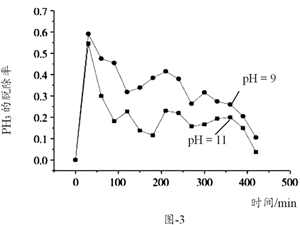
研究氮氧化物等大气污染物的处理对建设美丽家乡、打造宜居环境具有重要意义。
(1)Pb(NO3)2受热分解后能得到PbO、NO2和另一种气体,该气体为_______(写分子式)。
(2)现有以下反应:2H2(g)+O2(g)=2H2O(l)∆H1
N2(g)+O2(g)=2NO(g)∆H2
2H2(g)+2NO(g) =2H2O(l)+ N2(g) ∆H3
查阅资料获得部分化学键的键能E数据如下表:
| 化学键 |
|
|
|
|
| E/(kJ∙mol-1) | 946 | 436 | 497 | 632 |
已知∆H1=-572kJ/mol,则∆H3=________。
(3)O3-石灰乳联合处理NO的方法是先将NO经O3氧化,再用石灰乳吸收氮的氧化物,发生的主要化学反应有:NO+O3=NO2+O2,2NO+O2=2NO2,NO2+NO+Ca(OH)2= Ca(NO2)2+H2O,4NO2+2Ca(OH)2=Ca(NO3)2+Ca(NO2)2+2H2O,
①为保证NO被充分吸收,![]() 至少为_______(填字母)。
至少为_______(填字母)。
A.![]() B.
B.![]() C.
C.![]() D.1
D.1
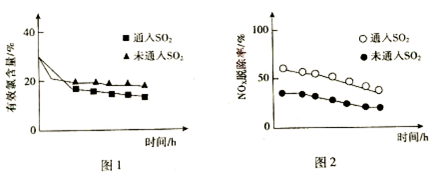
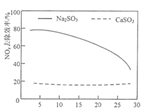
②其他条件相同时,石灰乳浆液中分别加入等物质的量的不同亚硫酸盐对NOx去除效率的影响如图所示。0~25min内,Na2SO3对NOx的去除效率明显高于CaSO3的原因是_______。
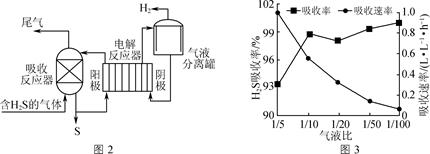
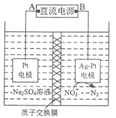
③下图是环保工业中利用催化反硝化电解法降解水中![]() 的示意图,写出阴极的电极反应式_______。
的示意图,写出阴极的电极反应式_______。
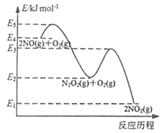
(4)对于反应2NO(g)+O2(g)⇌2NO2(g),有学者认为分两步完成,其反应历程如图所示。已知第1步反应2NO(g)⇌N2O2(g)(是快反应,会快速建立平衡状态,第2步反应N2O2(g)+O2(g)⇌2NO2(g)是慢反应。研究发现,在未使用催化剂的条件下,升高温度,总反应速率减慢,其原因可能是_______。
答案
O2 -751 kJ∙mol-1 B Na2SO3易溶于水,其溶液中亚硫酸根离子浓度较大,能够与NOx气体充分接触并加快反应速率,而亚硫酸钙难溶于水,其溶液中亚硫酸根离子的浓度较小 2![]() +10e-+12H+= N2+6H2O 决定总反应速率的是第2步反应,温度升高后,第1步反应为放热反应,平衡逆向移动,导致N2O2(g)的浓度减小,温度升高对于第2步反应的影响弱于N2O2(g)浓度的影响,N2O2(g)浓度的减小导致反应速率降低
+10e-+12H+= N2+6H2O 决定总反应速率的是第2步反应,温度升高后,第1步反应为放热反应,平衡逆向移动,导致N2O2(g)的浓度减小,温度升高对于第2步反应的影响弱于N2O2(g)浓度的影响,N2O2(g)浓度的减小导致反应速率降低
【解析】
(1)根据化合价升降进行判断;
(2)根据表中数据及化学键与焓变的关系计算;
(3)利用方程式的关系计算;
(4)利用温度与浓度的变化判断。
【详解】
(1)Pb(NO3)2受热分解得到PbO、NO2,Pb的化合价未变,而N的化合价降低,则O的化合价升高,另一种气体为氧气;
(2)根据表中数据及化学键与焓变的关系,∆H2=946 kJ∙mol-1+497 kJ∙mol-1-632kJ∙mol-1×2=+179kJ∙mol-1;根据盖斯定律,∆H3=∆H1-∆H2=-572 kJ∙mol-1-179kJ∙mol-1=-751 kJ∙mol-1;
(3)①根据方程式,n(NO):n(NO2)=1:1时,即可完全吸收且消耗O3的量最少。消耗1mol O3,生成3mol NO2,则共消耗6mol的NO,即n(O3):n(NO)=1:6,答案为B;
②根据图像可知,0~25min内,Na2SO3对NOx的去除效率明显高于CaSO3,Na2SO3易溶于水,其溶液中亚硫酸根离子浓度较大,能够与NOx气体充分接触并加快反应速率,而亚硫酸钙难溶于水,其溶液中亚硫酸根离子的浓度较小;
③根据图像可知,电解时,![]() 变为N2,化合价降低,得电子,作阴极,交换膜为质子交换膜,则阴极电极反应式为2
变为N2,化合价降低,得电子,作阴极,交换膜为质子交换膜,则阴极电极反应式为2![]() +10e-+12H+= N2+6H2O;
+10e-+12H+= N2+6H2O;
(4)根据图像可知,第1步反应与第2步反应均为放热反应,升高温度反应速率加快,研究发现,升高温度,总反应速率减慢,则升高温度第1步反应平衡逆向移动,导致N2O2(g)的浓度降低,对第2步反应,温度升高的影响弱于N2O2(g)的浓度的影响,则总反应速率减慢的原因为N2O2(g)的浓度的减小。