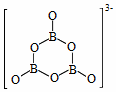
、
属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
键、
键。下列说法错误的是
A . 的熔点高于
B .晶体中所有化学键均为极性键
C .晶体中所有原子均采取 杂化 D .晶体中所有原子的配位数均相同
答案
A
【分析】 Al 和 Ga 均为第 ⅢA 元素, N 属于第 ⅤA 元素, AlN 、 GaN 的成键结构与金刚石相似,则其为共价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。 AlN 、 GaN 晶体中, N 原子与其相邻的原子形成 3 个普通共价键和 1 个配位键。
【详解】 A .因为 AlN 、 GaN 为结构相似的共价晶体,由于 Al 原子的半径小于 Ga , N—Al 的键长小于 N—Ga 的,则 N—Al 的键能较大,键能越大则其对应的共价晶体的熔点越高,故 GaN 的熔点低于 AlN , A 说错误;
B .不同种元素的原子之间形成的共价键为极性键,故两种晶体中所有化学键均为极性键, B 说法正确;
C .金刚石中每个 C 原子形成 4 个共价键(即 C 原子的价层电子对数为 4 ), C 原子无孤电子对,故 C 原子均采取 sp 3 杂化;由于 AlN 、 GaN 与金刚石互为等电子体,则其晶体中所有原子均采取 sp 3 杂化, C 说法正确;
D .金刚石中每个 C 原子与其周围 4 个 C 原子形成共价键,即 C 原子的配位数是 4 ,由于 AlN 、 GaN 与金刚石互为等电子体,则其晶体中所有原子的配位数也均为 4 , D 说法正确。
综上所述,本题选 A 。


 等。
等。  、金刚石等。
、金刚石等。  等。
等。  等。
等。  等。
等。  等。
等。  等。
等。  等原子晶体。
等原子晶体。  等)。
等)。