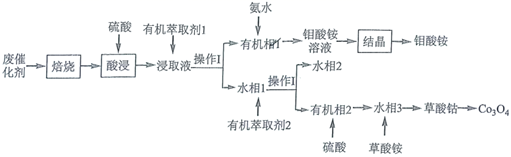
工业废弃物的资源化回收再利用,可以更大限度的发挥原材料的价值。下图是工业生产纳米磁性氧化铁的流程:
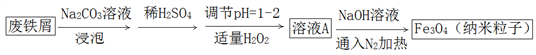
下列说法不正确的是
A.用Na2CO3溶液浸泡是为了除去废铁屑表面的铁锈
B.若生产中不通入N2,暴露在空气中生产,将不能得到高纯度产品
C.加适量的H2O2是为了将部分Fe2+氧化为Fe3+ ,涉及反应:H2O2+2Fe2++2H+=2Fe3++2H2O
D.溶液A中Fe2+和Fe3+的浓度比为1:2
答案
A
【详解】
A. Na2CO3溶液水解显碱性,浸泡废铁屑可以使表面的油脂水解除去,但不能除去表面的铁锈,故A错误;
B.废铁屑被硫酸溶解生成硫酸亚铁,生成的亚铁离子被双氧水部分氧化生成铁离子,形成亚铁离子和铁离子的混合溶液,若生产中不通入N2,暴露在空气中生产,亚铁离子会被空气中的氧气氧化生成铁离子,将不能得到高纯度四氧化三铁产品,其中会混入氧化铁杂质,故B正确;
C.根据B的分析,加适量的H2O2是为了将部分Fe2+氧化为Fe3+ ,涉及反应:H2O2+2Fe2++2H+=2Fe3++2H2O,故C正确;
D.根据最终产品为四氧化三铁,其中Fe2+和Fe3+的数目比为1:2,因此溶液A中Fe2+和Fe3+的浓度比为1:2,故D正确;
故选A。