酸性蚀刻液的主要成分是 H 2 O 2 /HCl ,腐蚀铜后的废液中主要含有 CuCl 2 、 HCl 。一种以废铝屑为主要原料回收酸性蚀刻废液中的铜并生产 AlCl 3 的工艺流程如下:
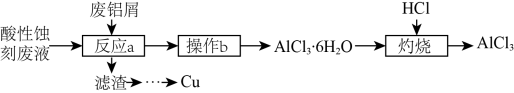
回答下列问题:
(1) 在实验室, “ 反应 a” 过程需远离火源,其原因是 _______( 用文字叙述 ) 。
(2)“ 操作 b” 包括 _______ 、过滤、洗涤,其中过滤需要用到的玻璃仪器有 _______ 、烧杯。
(3) 实验室可用食盐与浓硫酸在微热条件下反应制取 HCl 气体。
①HCl 气体的发生装置应选择装置 _______( 填字母,下同 ) ,用水吸收多余的 HCl 气体时,应该选择装置 _______ ,其原因是 _______ 。
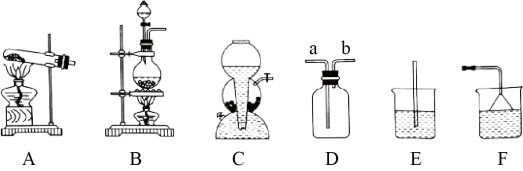
② 写出制备 HCl 反应的化学方程式: _______ ,该反应利用了浓 H 2 SO 4 的性质是 _______( 填 “ 脱水性 ”“ 氧化性 ” 或 “ 难挥发性 ”)
(4)“ 灼烧 ” 时,若在无 HCl 的气氛中反应,最终是否生成 给出判断并说明理由: _______ 。
答案
(1)Al 与稀 HCl 反应产生 ,其遇明火易发生爆炸
(2) 蒸发浓缩、冷却结晶 漏斗、玻璃棒
(3) B F HCl 易溶于水,选择 F 可防止倒吸 ( 浓 )
难挥发性
(4) 不能生成 ,因为
水解,生成 HCl 易挥发,导致平衡
右移生成
,灼烧生成
【分析】酸性蚀刻废液即腐蚀铜后的废液中主要含有 CuCl 2 、 HCl ,加入废铝屑后发生的反应 a 有: 2Al+6HCl=2AlCl 3 +3H 2 ↑ , 2Al+3CuCl 2 =2AlCl 3 +3Cu ,过滤后得到滤渣主要成分为 Al 和 Cu ,加入足量的盐酸后除去 Al ,再过滤洗涤得到 Cu ,滤液中主要含有 AlCl 3 溶液,经过蒸发浓酸、冷却结晶,过滤洗涤干燥得到 AlCl 3 ·6H 2 O 晶体,在 HCl 的气流中进行灼烧可得无水 AlCl 3 ,据此分析解题。
( 1 )
由分析可知,反应 a 有: 2Al+6HCl=2AlCl 3 +3H 2 ↑ , 2Al+3CuCl 2 =2AlCl 3 +3Cu , Al 与稀 HCl 反应产生 ,其遇明火易发生爆炸,故在实验室, “ 反应 a” 过程需远离火源,故答案为: Al 与稀 HCl 反应产生
,其遇明火易发生爆炸;
( 2 )
由分析可知, “ 操作 b” 包括蒸发浓缩、冷却结晶、过滤、洗涤,其中过滤需要用到的玻璃仪器有漏斗、玻璃棒、烧杯,故答案为:蒸发浓缩、冷却结晶;漏斗、玻璃棒;
( 3 )
① 由题干信息可知,制备 HCl 采用固液加热装置,个 HCl 气体的发生装置应选择装置 B ,由于 HCl 易溶于水,用水吸收多余的 HCl 气体时,需考虑倒吸现象的发生,而选择 F 可防止倒吸,故答案为: B ; F ; HCl 易溶于水,选择 F 可防止倒吸;
② 由题干信息可知,制备 HCl 反应的化学方程式为: NaCl+H 2 SO 4 ( 浓 ) NaHSO 4 +HCl↑ ,该反应利用了浓 H 2 SO 4 的性质是难挥发性,故答案为: NaCl+H 2 SO 4 ( 浓 )
NaHSO 4 +HCl↑ ;难挥发性;
( 4 )
因为 水解,生成 HCl 易挥发,导致平衡
右移生成
,灼烧生成
, “ 灼烧 ” 时,若在无 HCl 的气氛中反应,最终不能生成
, 故答案为:不能生成
,因为
水解,生成 HCl 易挥发,导致平衡
右移生成
,灼烧生成
。

