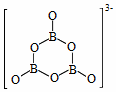
下列表述中正确的是
A . 碳碳双键中有 1 个 键、 1 个
键,碳碳三键中有 1 个
键、 2 个
键
B . 因为 H — O 键的键能小于 H — F 键的键能,所以 、
与
的反应能力逐渐减弱
C . 水分子的结构可表示为 H — O — H ,分子中的键角为 180 °
D . 沸点:邻羟基苯甲醛>对羟基苯甲醛
答案
A
【详解】
A .双键、三键中均只含 1 个 σ 键,其余为 π 键,则碳碳双键中有一个 σ 键,一个 π 键,碳碳叁键中有一个 σ 键,两个 π 键,故 A 正确;
B . H-O 键的键能小于 H-F 键的键能,则稳定性: HF > H 2 O ,所以 O 2 、 F 2 与 H 2 反应的能力逐渐增强,故 B 错误;
C .水分子结构式可表示为 H-O-H ,但空间构型是 V 形,不是直线形,分子中的键角大约为 105° ,故 C 错误;
D .对羟基苯甲醛易形成分子间氢键,邻羟基苯甲醛易形成分子内氢键,则邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,故 D 错误;
故选: A 。


 等。
等。  、金刚石等。
、金刚石等。  等。
等。  等。
等。  等。
等。  等。
等。  等。
等。  等原子晶体。
等原子晶体。  等)。
等)。