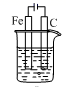
下列说法正确的是( )
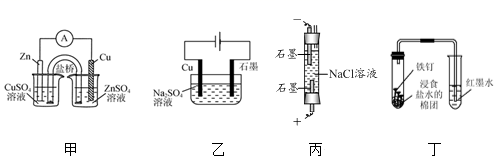
A.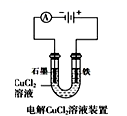 中阳极处能产生使湿润淀粉KI试纸变蓝的气体
中阳极处能产生使湿润淀粉KI试纸变蓝的气体
B.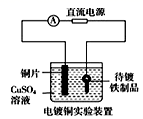 中待镀铁制品应与电源正极相连
中待镀铁制品应与电源正极相连
C.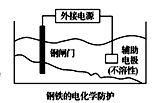 中钢闸门应与外接电源的正极相连,称为牺牲阳极的阴极保护法
中钢闸门应与外接电源的正极相连,称为牺牲阳极的阴极保护法
D. 中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
答案
D
【详解】
A.在阳极Fe失去电子变为Fe2+进入溶液,Fe2+与KI不能发生反应,因此不能产生使湿润淀粉KI试纸变蓝的气体,A错误;
B.电镀时,应该把待镀铁制品与电源负极相连,作阴极,发生还原反应,B错误;
C.钢闸门应与外接电源的负极相连,称为外接电流的阴极保护法,C错误;
D.根据图示可知:该离子交换膜可以使Na+通过,而不能使Cl2通过,因此就可以避免生成的Cl2与NaOH溶液反应,D正确;
故合理选项是D。




 B
B C
C D
D