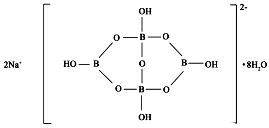
X是合成碳酸二苯酯的一种有效的氧化还原催化助剂,可由EDTA与Fe3+反应得到。

(1)EDTA中碳原子杂化轨道类型为______;EDTA中四种元素的电负性由小到大的顺序为________。
(2)Fe3+基态外围电子排布式为______。
(3)EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点(540.6 ℃)比正二十一烷的沸点(100 ℃)高的原因是______。
(4)1 mol 碳酸分子中含有σ键的数目为______。
(5)X中的配位原子是______。
答案
sp2和sp3 H < C < N < O 3d5 EDTA分子间存在氢键 5 mol N、O
【解析】
(1)EDTA中羧基上C原子价层电子对个数是3、亚甲基上C原子价层电子对个数是4,根据价层电子对互斥理论判断C原子杂化轨道类型,前者为sp2杂化、后者为sp3 杂化,元素的非金属性越强,其电负性越大,非金属性H<C<N<O,则电负性H<C<N<O。
(2)Fe原子失去3个电子生成铁离子,根据构造原理书写铁离子核外电子排布式为[Ar]3d5,外围电子排布式为3d5。
(3)能形成分子间氢键的物质熔沸点较高,EDTA能形成分子间氢键,导致其熔沸点较高。
(4)共价单键为σ键,共价双键中含有一个σ键、一个π键,1个碳酸分子中含有两个氧氢单键、两个碳氧单键和一个碳氧双键,故1 mol 碳酸分子中含有σ键的数目为5NA。
(5)X中N、O原子提供孤电子对,所以N、O为配位原子。