亚硝酸钠是重要的防腐剂。某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验)
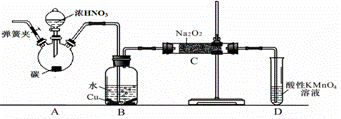
查阅资料:①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②在酸性溶液中,NO2-可将MnO4-还原为Mn2+且无气体生成。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
实验操作:①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;
③从C中取少量固体,检验是否是亚硝酸钠。
(1)A中反应的化学方程式是 。
(2)B中观察的主要现象是 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的操作是 。
(4)经检验C产物中亚硝酸钠含量较少。
a.甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠。
生成碳酸钠的化学方程式是 。为排除干扰甲在B、C装置间增加装置E,E中盛放的试剂应是 (写名称)。
b.乙同学认为除上述干扰因素外,还会有空气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是 。
(5)实验经改进后可制得较纯亚硝酸钠,下列说法正确的是 。
a.亚硝酸钠有咸味,可代替食盐食用
b.常温下,0.1mol/L亚硝酸溶液pH>1
c.已知亚硝酸电离平衡常数为Ka;亚硝酸根水解常数为Kh;水的离子积为Kw;则三者关系为:Ka·Kh=Kw
d.0.1mol/L亚硝酸钠溶液中存在:c(NO2-)>c(Na+)>c(OH-)>c(H+)
答案
【答案】(1)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;(2)溶液变蓝,铜片溶解,无色气体冒出;除去未反应的NO,防止污染空气(3)将生成物置于试管中,加入稀硫酸,若产生无色气体并在液面上方变为红棕色,则D中产物是亚硝酸钠。(反应的离子方程式是3NO2-+2H+=NO3-+2NO↑+H2O)或者:将生成物置于试管中,加入酸性KMnO4溶液,若无气泡产生,溶液紫色褪去,则D中产物是亚硝酸钠,(反应的离子方程式是5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O)a.2CO2+2Na2O2===2Na2CO3+O2,碱石灰(1分)b.打开弹簧夹,通入N2一段时间(5)bc
CO2↑+4NO2↑+2H2O;(2)溶液变蓝,铜片溶解,无色气体冒出;除去未反应的NO,防止污染空气(3)将生成物置于试管中,加入稀硫酸,若产生无色气体并在液面上方变为红棕色,则D中产物是亚硝酸钠。(反应的离子方程式是3NO2-+2H+=NO3-+2NO↑+H2O)或者:将生成物置于试管中,加入酸性KMnO4溶液,若无气泡产生,溶液紫色褪去,则D中产物是亚硝酸钠,(反应的离子方程式是5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O)a.2CO2+2Na2O2===2Na2CO3+O2,碱石灰(1分)b.打开弹簧夹,通入N2一段时间(5)bc




