下列设备工作时,将化学能转化为电能的是()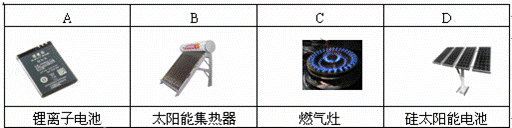
A. A B. B C. C D. D
考点: 原电池和电解池的工作原理.
专题: 电化学专题.
分析: 将化学能转化为电能,应为原电池装置,结合能量的转化特点判断.
解答: 解:A.锂离子电池是化学能转化为电能的装置,为原电池,故A正确;
B.太阳能集热器为太阳能转化为热能的装置,故B错误;
C.燃气灶为化学能转化为热能的装置,故C错误;
D.硅太阳能电池为太阳能转化为电能的装置,故D错误.
故选A.
点评: 本题考查原电池和电解池知识,侧重于学生的分析能力和电化学知识的综合考查,为2015届高考常见题型和高频考点,注意把握常见能量的转化形成,难度不大.
下列说法中,不正确的是()
A. 碘是人体必需的微量元素之一
B. 碳酸氢钠可用于治疗胃酸过多
C. 肉类富含蛋白质,属于碱性食物
D. 食用富含维生素C的水果有益于身体健康
考点: 微量元素对人体健康的重要作用;维生素在人体中的作用;人体新陈代谢过程中的生化反应;常见的食品添加剂的组成、性质和作用.
专题: 有机化学基础.
分析: A.人体必需的微量元素主要有:铁、钴、铜、锌、铬、锰、钼、氟、碘、硒;
B.碳酸氢钠可以和胃液中的盐酸反应;
C.食品的酸碱性与其本身的pH值无关(味道是酸的食品不一定是酸性食品),主要是食品经过消化、吸收、代谢后,最后在人体内变成酸性或碱性的物质来界定;
D.生素可以调节新陈代谢、维持身体健康.
解答: 解:A.碘是人体必需的微量元素,故A正确;
B.碳酸氢钠可以用于治疗胃酸过多,因为碳酸氢钠可以和胃液中的盐酸反应,故B正确;
C.含氮、碳、硫、氯、等元素较多的食物,经过消化形成酸根留在体内,产生酸性物质的称为酸性食品,如淀粉类;动物性食物;甜食;油炸食物或奶油类;豆类(如花生等),故C错误;
D.维生素可以调节新陈代谢、维持身体健康,蔬菜、水果中含有丰富的维生素,故D正确.
故选C.
点评: 本题考查微量元素、抗酸药、食物酸碱性和维生素等,题目难度不大,注意基础知识的积累.
下列物质中,既含离子键又含共价键的是()
A. NaCl B. CO2 C. NaOH D. N2
考点: 共价键的形成及共价键的主要类型;离子化合物的结构特征与性质.
专题: 化学键与晶体结构.
分析: 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,既含离子键、又含共价键的物质应为离子化合物,并且含有由多个原子组成的阴离子,据此分析解答.
解答: 解:A.氯化钠只含离子键,故A错误;
B,二氧化碳中只含共价键,故B错误;
C.氢氧化钠中钠离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在共价键,故C正确;
D.氮气中只含共价键,故D错误;
故选C.
点评: 本题考查化学键知识,题目难度不大,注意离子键与共价键的区别.
设NA为阿伏伽德罗常数的值,下列说法正确的是()
A. 7.8g Na2O2中离子总数为0.4NA
B. 标准状况下,11.2L CCl4中的分子数为0.5NA
C. 常温常压下,48g O2和O3的混合气体中含有的氧原子数为3NA
D. 2.7g金属铝变为铝离子时失去的电子数为0.1NA
考点: 阿伏加德罗常数.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A.7.8g过氧化钠的物质的量为0.1mol,0.1mol过氧化钠中含有0.2mol钠离子、0.1mol过氧根离子;
B.标况下,四氯化碳不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
C.48g臭氧和氧气中含有48g氧原子,含有3mol氧原子;
D.铝为3价金属,2.7g铝的物质的量为0.1mol,变成铝离子时失去0.3mol电子.
解答: 解:A.过氧化钠中阴离子为过氧根离子,7.8g过氧化钠的物质的量为0.1mol,0.1mol过氧化钠中含有0.2mol钠离子、0.1mol过氧根离子,总共含有0.3mol离子,离子总数为0.3NA,故A错误;
B.标况下四氯化碳不是气体,题中条件无法计算四氯化碳的物质的量,故B错误;
C.48g氧气和臭氧的混合物中含有48gO原子,含有氧原子的物质的量为3mol,含有的氧原子数为3NA,故C正确;
D.2.7g铝的物质的量为0.1mol,0.1mol铝变成铝离子失去0.3mol电子,失去的电子数为0.3NA,故D错误;
故选C.
点评: 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下四氯化碳不是气体、过氧化钠中阴离子为过氧根离子.
下列化学用语表示不正确的是()
A. Na+的结构示意图 ![]() B. 四氯化碳的电子式
B. 四氯化碳的电子式 ![]()
C. 二氧化碳的结构式为O=C=O D. 乙烯的实验式为 CH2
考点: 电子式、化学式或化学符号及名称的综合.
专题: 化学用语专题.
分析: A.钠离子的核电荷数为11,核外电子总数为10,最外层达到8电子稳定结构;
B.四氯化碳分子中,氯原子最外层达到8电子稳定结构,漏掉了氯原子的3对未成键电子;
C.二氧化碳为直线型结构,分子中存在两个碳氧双键;
D.乙烯的分子式为:C2H4,根据其分子式写出其实验式.
解答: 解:A.钠离子与钠原子的核电荷数都是11,钠离子最外层电子为8,核外电子总数为10,钠离子的结构示意图为:![]() ,故A正确;
,故A正确;
B.四氯化碳为共价化合物,氯原子和碳原子最外层都达到8电子稳定结构,四氯化碳正确的电子式为: ,故B错误;
,故B错误;
C.二氧化碳为共价化合物,分子中存在两个碳氧双键,且为直线型结构,二氧化碳的结构式为:O=C=O,故C正确;
D.实验式又称为最简式,是分子中各原子的最简比,乙烯的分子式为:C2H4,则其实验式为CH2,故D正确;
故选B.
点评: 本题考查了电子式、离子结构示意图、结构式、实验式的表示方法判断,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确实验式、分子式、结构式、电子式的区别,试题培养了学生灵活应用所学知识的能力.
本卷还有22题,登录并加入会员即可免费使用哦~

该作品由: 用户蒋拓分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。