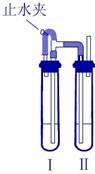
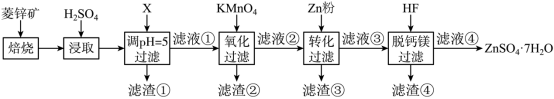
硫酸锌 (ZnSO 4 ) 是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 ZnCO 3 ,杂质为 SiO 2 以及 Ca 、 Mg 、 Fe 、 Cu 等的化合物。其制备流程如下:
本题中所涉及离子的氢氧化物溶度积常数如下表:
| 离子 | | | | | |
| | | | | | |
回答下列问题:
(1) 菱锌矿焙烧生成氧化锌的化学方程式为 。
(2) 为了提高锌的浸取效果,可采取的措施有 、 。
(3) 加入物质 X 调溶液 ,最适宜使用的 X 是 ( 填标号 ) 。
A . B .
C .
滤渣 ① 的主要成分是 、 、 。
(4) 向 的滤液 ① 中分批加入适量
溶液充分反应后过滤,滤渣 ② 中有
,该步反应的离子方程式为 。
(5) 滤液 ② 中加入锌粉的目的是 。
(6) 滤渣 ④ 与浓 反应可以释放 HF 并循环利用,同时得到的副产物是 、 。
答案
(1)ZnCO 3 ZnO+CO 2 ↑
(2) 将焙烧后的产物碾碎,增大接触面积 增大硫酸的浓度等
(3) B Fe(OH) 3 CaSO 4 SiO 2
(4)3Fe 2+ + +7H 2 O=3Fe(OH) 3 ↓+MnO 2 ↓+5H +
(5) 置换 Cu 2+ 为 Cu 从而除去
(6) CaSO 4 MgSO 4
【分析】由题干信息,菱锌矿的主要成分为 ZnCO 3 ,杂质为 SiO 2 以及 Ca 、 Mg 、 Fe 、 Cu 等的化合物,结合流程图分析,菱锌矿焙烧,主要发生反应 ZnCO 3 ZnO+CO 2 ↑ ,再加入 H 2 SO 4 酸浸,得到含 Zn 2+ 、 Ca 2+ 、 Mg 2+ 、 Fe 2+ 、 Fe 3+ 、 Cu 2+ 的溶液,加入物质 X 调节 pH=5 ,结合表格数据,过滤得到 Fe(OH) 3 、 CaSO 4 、 SiO 2 的滤渣 ① ,滤液 ① 中主要含有 Zn 2+ 、 Cu 2+ 、 Mg 2+ 、 Ca 2+ 、 Fe 2+ ,再向滤液 ① 中加入 KMnO 4 溶液氧化 Fe 2+ ,过滤得到 Fe(OH) 3 和 MnO 2 的滤渣 ② ,滤液 ② 中加入锌粉,发生反应 Zn+Cu 2+ =Zn 2+ +Cu ,过滤后得到滤渣 ③ 为 Cu ,再向滤液 ③ 中加入 HF 脱钙镁,过滤得到滤渣 ④ 为 CaF 2 、 MgF 2 ,滤液 ④ 为 ZnSO 4 溶液,经一系列处理得到 ZnSO 4 ·7H 2 O ,据此分析解答。
【详解】( 1 )由分析,焙烧时,生成 ZnO 的反应为: ZnCO 3 ZnO+CO 2 ↑ ;
( 2 )可采用将焙烧后的产物碾碎,增大接触面积、增大硫酸的浓度等方式提高锌的浸取率;
( 3 ) A . NH 3 ·H 2 O 易分解产生 NH 3 污染空气,且经济成本较高,故 A 不适宜;
B . Ca(OH) 2 不会引入新的杂质,且成本较低,故 B 适宜;
C . NaOH 会引入杂质 Na + ,且成本较高, C 不适宜;
故答案选 B ;
当沉淀完全时 ( 离子浓度小于 10 -5 mol/L) ,结合表格 Ksp 计算各离子完全沉淀时 pH < 5 的只有 Fe 3+ ,故滤渣 ① 中有 Fe(OH) 3 ,又 CaSO 4 是微溶物, SiO 2 不溶于酸,故滤渣 ① 的主要成分是 Fe(OH) 3 、 CaSO 4 、 SiO 2 ;
( 4 )向 80~90℃ 滤液 ① 中加入 KMnO 4 溶液,可氧化 Fe 2+ ,得到 Fe(OH) 3 和 MnO 2 的滤渣 ② ,反应的离子方程式为 3Fe 2+ + +7H 2 O=3Fe(OH) 3 ↓+MnO 2 ↓+5H + ;
( 5 )滤液 ② 中加入锌粉,发生反应 Zn+Cu 2+ =Zn 2+ =Cu ,故加入锌粉的目的为置换 Cu 2+ 为 Cu 从而除去;
( 6 )由分析,滤渣 ④ 为 CaF 2 、 MgF 2 ,与浓硫酸反应可得到 HF ,同时得到的副产物为 CaSO 4 、 MgSO 4 。