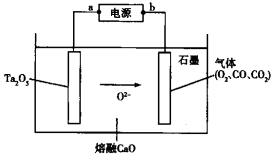
一种水性电解液 Zn-MnO 2 离子选择双隔膜电池如图所示 (KOH 溶液中, Zn 2+ 以 Zn(OH) 存在 ) 。电池放电时,下列叙述错误的是

A . Ⅱ 区的 K + 通过隔膜向 Ⅲ 区迁移
B . Ⅰ 区的 SO 通过隔膜向 Ⅱ 区迁移
C . MnO 2 电极反应: MnO 2 +2e - +4H + =Mn 2+ +2H 2 O
D .电池总反应: Zn+4OH - +MnO 2 +4H + =Zn(OH) +Mn 2+ +2H 2 O
答案
A
【分析】根据图示的电池结构和题目所给信息可知, Ⅲ 区 Zn 为电池的负极,电极反应为 Zn-2e - +4OH - =Zn(OH) , Ⅰ 区 MnO 2 为电池的正极,电极反应为 MnO 2 +2e - +4H + =Mn 2+ +2H 2 O ;电池在工作过程中,由于两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此可以得到 Ⅰ 区消耗 H + ,生成 Mn 2+ , Ⅱ 区的 K + 向 Ⅰ 区移动或 Ⅰ 区的 SO
向 Ⅱ 区移动, Ⅲ 区消耗 OH - ,生成 Zn(OH)
, Ⅱ 区的 SO
向 Ⅲ 区移动或 Ⅲ 区的 K + 向 Ⅱ 区移动。据此分析答题。
【详解】 A .根据分析, Ⅱ 区的 K + 只能向 Ⅰ 区移动, A 错误;
B .根据分析, Ⅰ 区的 SO 向 Ⅱ 区移动, B 正确;
C . MnO 2 电极的电极反应式为 MnO 2 +2e - +4H + =Mn 2+ +2H 2 O , C 正确;
D .电池的总反应为 Zn+4OH - +MnO 2 +4H + =Zn(OH) +Mn 2+ +2H 2 O , D 正确;
故答案选 A 。