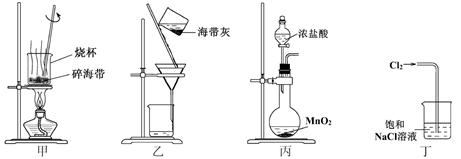
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
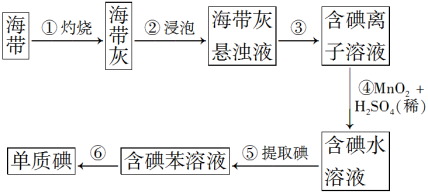
请填写下列空白:
(1) 步骤 ① 灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是 _______( 从下列仪器中选出所需的仪器,将标号字母填写在空白处 ) 。
A .烧杯 B .表面皿 C .坩埚 D .酒精灯 E. 干燥器
(2) 步骤 ④ 一定发生的化学反应类型是 _______ 。
A .化合反应 B .分解反应 C .氧化还原反应
(3) 步骤 ⑤ 所用的主要仪器是 _______ 。步骤 ③ 的实验操作名称是 _______ 。
(4)① ~ ⑥ 操作中,使用玻璃棒的是 _______( 填序号 ) 。
(5) 请设计简单实验,验证 ⑤ 提取碘后的水溶液中是否含有碘单质 _______ 。
答案
(1)CD
(2)C
(3) 分液漏斗、烧杯 过滤
(4)①②③
(5) 取少量提取碘后的水溶液于试管中,加入几滴淀粉试液,观察是否出现蓝色 ( 如果变蓝,说明还有单质碘 )
【分析】实验室从海带中提取碘: ① 海带灼烧成灰, ② 浸泡溶解得到海带灰悬浊液, ③ 过滤,得到滤液为含碘离子的溶液, ④ 滤液中加入酸和氧化剂 MnO 2 ,将碘离子氧化成碘单质, ⑤ 利用有机溶剂苯萃取分液得到碘的苯溶液, ⑥ 通过蒸馏提取出碘单质,据此解答。
( 1 )
灼烧固体物质一般用酒精灯加热坩埚,坩埚用泥三脚支撑、置于三脚架上,则步骤 ① 灼烧海带时,除需要三脚架、泥三角外,还需要用到下列仪器中坩埚和酒精灯,则选 CD 。
( 2 )
步骤 ④ 碘离子被 MnO 2 氧化成碘单质,则一定发生的化学反应类型是氧化还原反应;
选 C 。
( 3 )
步骤 ⑤ 利用有机溶剂苯萃取并分液得到碘的苯溶液,则所用的主要仪器是分液漏斗、烧杯。步骤 ③ 为固液分离,实验操作名称是过滤。
( 4 )
① ~ ⑥ 操作中, ① 灼烧需要用玻璃棒搅拌固体、 ② 浸泡时玻璃棒起搅拌作用、 ③ 过滤时玻璃棒起引流作用,则使用玻璃棒的是 ①②③ 。
( 5 )
提取碘后的水溶液中若是含有单质碘,则遇到淀粉会变蓝色,故答案为:可以取少量提取碘后的水溶液于试管中,加入几滴淀粉试液,观察是否出现蓝色 ( 如果变蓝,说明还有单质碘 ) 。