SCR 催化剂广泛应用于燃煤烟气的处理,其主要成分为 、
、
,还含有少量 CaO 、
、
等。一种从废 SCR 催化剂中回收钨的工艺如下:
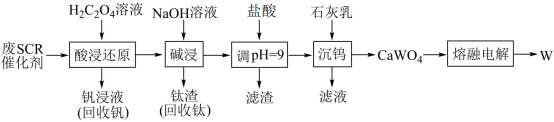
(1)“ 酸浸还原 ” 中 转化成可溶于水的
,该反应的化学方程式为 _______ 。
(2)“ 碱浸 ” 时 转化为
的离子方程式为 _______ 。
(3)“ 滤渣 ” 的主要成分是 _______ 。
(4) 常温下 ,
。 “ 沉钨 ” 过程中不断加入石灰乳,当 “ 滤液 ” 的
时,
为 _______
。
(5)“ 熔融电解 ” 过程中阴极反应为 。电解过程中作阳极的石墨易消耗,原因是 _______ 。
(6) 钛渣经处理可得到粗 。将
氯化为
是冶炼金属钛的主要反应之一、工业上常采用 “ 加碳氯化 ” 的方法生产
,同时得到 CO ,相应的化学方程式为
①
②
结合数据说明氯化过程中加碳的理由 _______ 。
答案
(1)
(2)
(3)Al(OH) 3
(4)1.6 10 -5
(5) 石墨此时作阳极,发生氧化反应,生成了 CO 2 ,石墨被消耗
(6)
,反应的
,
,
,使反应得以进行
【分析】由流程图可知,废 SCR 催化剂(主要成分为 、
、
,还含有少量 CaO 、
、
等),加入
溶液酸浸还原,
转化成可溶于水的
,过滤后,所得钒浸液可回收钒;所得固体再加入 NaOH 溶液碱浸,
转化为
,过滤后,所得钛渣含有
、
等不溶物,可回收钛;向碱浸液加入盐酸调溶液 pH=9 ,溶液中的
转化为 Al(OH) 3 沉淀,过滤后,向滤液中加入石灰乳沉钨,得到
,电解熔融
得到 W 。
( 1 )
与
反应得到
,该反应中 V 元素化合价从 +5 变为 +4 ,则 C 元素化合价从 +3 变为 +4 ,说明反应中有 CO 2 生成,其反应的化学方程式为
,故答案为:
;
( 2 )
“ 碱浸 ” 时 与
反应生成了
,故反应的离子方程式为
,故答案为:
;
( 3 )
用盐酸调解溶液 pH=9 时,溶液中的 转化为 Al(OH) 3 沉淀,故 “ 滤渣 ” 的主要成分是 Al(OH) 3 ,故答案为: Al(OH) 3 ;
( 4 )
此时溶液的 ,故 c(OH - )=0.1mol/L ,根据
可计算出 c(Ca 2+ )=5.5
10 -4 mol/L ,由
可计算出
=1.6
10 -5
,故答案为: 1.6
10 -5 ;
( 5 )
电解过程中作阳极的石墨易消耗,原因是石墨此时作阳极,发生氧化反应,生成了 CO 2 ,石墨被消耗,故答案为:石墨此时作阳极,发生氧化反应,生成了 CO 2 ,石墨被消耗;
( 6 )
已知: ①
;
②
;
根据盖斯定律, ①+② 得
,反应的
,
,
,使反应得以进行,故答案为:
,反应的
,
,
,使反应得以进行。

 ” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。
” 水解是吸热过程,是中和反应的逆过程。一般,水解的程度较小,写离子方程式时,不能用“↑”或“↓”符号。多元弱酸根分步水解,以第一步为主。多元弱碱阳离子一步水解。 

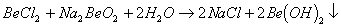 能完全进行,则下列推断中,正确的是
能完全进行,则下列推断中,正确的是 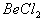 溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO
溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO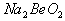 溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO
溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO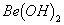 既能溶于盐酸又能溶于烧碱溶液
既能溶于盐酸又能溶于烧碱溶液