焦亚硫酸钠 (Na 2 S 2 O 5 ) 是常用的抗氧化剂,在空气中、受热时均易分解。
(1) 已知 Na 2 S 2 O 5 中 O 元素的化合价为 -2 ,则 S 元素的化合价为 _______ 。 Na 2 S 2 O 5 在酸性条件下会放出 SO 2 ,其反应的离子方程式为 _______ 。
(2)Na 2 S 2 O 5 是一种食品添加剂、 Na 2 S 2 O 5 晶体中常含有 。
①Na 2 S 2 O 5 作脱氧剂时的反应原理为 ,用单线桥法标出该反应中电子转移的数目和方向: _______ 。
② 检验其中含有 的方法是 _______ 。
(3) 葡萄酒中常加入 Na 2 S 2 O 5 作抗氧化剂。测定某葡萄酒中 Na 2 S 2 O 5 残留量的实验方法如下:取 20.00mL 葡萄酒样品,慢慢滴加 5.00mL0.010mol/LI 2 标准液恰好反应 ( 以淀粉溶液作指示剂 ) 。已知实验过程中发生的反应为 。计算该葡萄酒中 Na 2 S 2 O 5 的残留量为 _______mol/L 。
答案
(1) +4
(2) 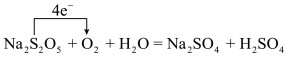 取少量晶体溶于水,加入稀盐酸酸化,滴加 BaCl 2 溶液,若产生白色沉淀,则有 SO
取少量晶体溶于水,加入稀盐酸酸化,滴加 BaCl 2 溶液,若产生白色沉淀,则有 SO
(3)1.25×10 -3
【解析】
(1)
化合物各元素化合价代数和为零,设 S 元素化合价为 x , ,解之得 x=+4 ;反应前后 S 元素化合价均是 +4 价,所以在酸性环境下发生简单的强酸制弱酸的离子反应,故离子方程式是
;
(2)
单线桥法表示电子转移,从反应物失电子元素引出,指向反应物中得电子元素,线桥上不标得失,只标注转移电子总量,所以本问第一空应填 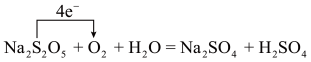 ;
; 检验要排除很多干扰离子,所以检验方法是:取少量晶体溶于水,加入稀盐酸酸化,滴加 BaCl 2 溶液,若产生白色沉淀,则有
;
(3)
设葡萄酒中 Na 2 S 2 O 5 的残留量浓度是 x ,根据题目所给信息,列式计算
,
解之,得 x=1.25×10 -3 mol•L -1 。



