下列图示与对应的叙述相符的是
| | | | |
| A .室温下,往盐酸中慢慢滴加蒸馏水时导电能力的变化 | B .往某浓度的 | C .室温下,往 20mLNaOH 溶液中滴加等浓度的 | D .石墨转化为金刚石的能量变化 |
A . A B . B C . C D . D
B
【解析】
【详解】
A .溶液的导电能力取决于自由移动离子浓度,往盐酸中慢慢滴加蒸馏水,溶液中离子浓度降低,溶液导电性减弱,故 A 不选;
B .向 AlCl 3 溶液中加入 NH 3 ⋅H 2 O ,产生 Al(OH) 3 沉淀,随着氨水的不断加入,沉淀的质量不断增大,当 AlCl 3 反应完时,沉淀质量达到最大,再滴入氨水, Al(OH) 3 不溶于氨水,所以沉淀质量不再变化,故 B 选;
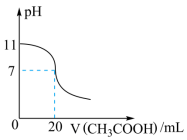
C .室温下,往 20mLNaOH 溶液中滴加等浓度的 CH 3 COOH ,当加入的醋酸体积为 20mL 时,溶质为 CH 3 COONa ,溶液显碱性,不显中性,故 C 不选;
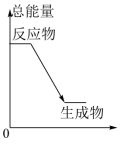
D .金刚石的能量比石墨高,石墨转化为金刚石需要吸收能量,能量应升高,故 D 不选;
故选 B 。
下列离子方程式正确的是
A .向硝酸溶液中加入 Na 2 SO 3 溶液 SO +2H + =SO 2 ↑ +H 2 O
B . Cu 与浓硝酸共热 : Cu + 4H + +2NO =Cu 2+ +2NO 2 ↑ +2H 2 O
C . FeO 加入稀硝酸: FeO+2H + =Fe 2+ +H 2 O
D . Cu 与浓硫酸共热: Cu+4H + +SO =SO 2 ↑+Cu 2+ + 2H 2 O
B
【解析】
【详解】
A .向硝酸溶液中加入 Na 2 SO 3 溶液,两者发生氧化还原反应,亚硫酸根被氧化为硫酸根,硝酸被还原为一氧化氮,故 A 错误;
B . Cu 与浓硝酸共热反应生成硝酸铜、二氧化氮和水,其离子方程式为: Cu + 4H + +2NO
Cu 2+ +2NO 2 ↑ +2H 2 O ,故 B 正确;
C . FeO 加入稀硝酸,氧化亚铁被硝酸氧化为铁离子: 3FeO+10H + +NO =3Fe 3+ +NO↑ +5H 2 O ,故 C 错误;
D . Cu 与浓硫酸共热生成硫酸铜、二氧化硫和水,浓硫酸以分子形式存在,不能拆,其离子方程式为: Cu+2H 2 SO 4 ( 浓 ) SO 2 ↑+Cu 2+ + 2H 2 O+SO
,故 D 错误;
综上所述,答案为 B 。
某一混合物的水溶液可能含有以下离子中的若干种: 、
、
、
、
、
。现取两份 100mL 的该溶液进行如下实验:
(1) 第一份加足量 溶液,加热,收集到标准状况下的气体
;
(2) 第二份加足量 溶液,得沉淀 4.30g ,再用足量盐酸洗涤,干燥后,沉淀质量为 2.33g 。
根据上述实验,下列推测正确的是
A . 一定存在
B . 该溶液中含
C . 不一定存在
D . 不确定,可向原溶液中加入
溶液进行检验
B
【解析】
【分析】
第一份加足量 溶液,加热,收集到标准状况下的气体
,说明含有铵根离子且物质的量为 0.02mol ;第二份加足量
溶液,得沉淀 4.30g ,再用足量盐酸洗涤,干燥后,沉淀质量为 2.33g ,得到硫酸钡质量为 2.33g ,碳酸钡质量为 1.97g ,说明含有硫酸根且物质的量为 0.01mol ,还含有碳酸氢根且物质的量为 0.01mol ,也说明原溶液中不含钡离子,根据电荷守恒,说明溶液中含有钠离子。
【详解】
A .根据前面分析 一定不存在,故 A 错误;
B .根据碳酸钡质量为 1.97g ,推出 该溶液中含
,故 B 正确;
C .根据电荷守恒,说明 一定存在,故 C 错误;
D . 不确定,原溶液中含有硫酸根和碳酸氢根,向原溶液中加入
溶液,不能检验出是否含有氯离子,主要是生成的硫酸银沉淀也是白色沉淀,故 D 错误。
综上所述,答案为 B 。
有一包白色粉末,可能含有 中的一种或几种,取少量样品进行如下实验:
① 溶于水,得无色澄清溶液;
② 向 ① 所得溶液中加入过量硝酸酸化的 溶液,有气体和沉淀产生。
则原白色粉末中一定含有的是
A . 、
B .
、 NaCl
C . 、
、 NaCl D .
、 NaCl
D
【解析】
【详解】
① 溶于水,得无色澄清溶液,说明不含有 CuSO 4 ; ② 向 ① 所得溶液中加入过量硝酸酸化的 溶液,有气体和沉淀产生,说明一定含有
,碳酸根离子和钙离子不共存,则
一定不存在, NaCl 一定含有,则原白色粉末中一定含有
、 NaCl ,故选: D 。
对于下列实验,能正确描述其反应的离子方程式的是
A .等浓度等体积的 溶液与
溶液混合:
B .向 溶液中滴加少量的酸性
溶液:
C .向 “84” 消毒液中滴加足量的稀硫酸:
D .向澄清石灰水中通入足量的 :
C
【解析】
【详解】
A .亚硫酸是弱酸, 不能拆成
、 H + 和
,应拆成
和
,等浓度等体积的
溶液与
溶液混合的离子方程式为:
,故 A 错误;
B .向 溶液中滴加少量的酸性
溶液, H 2 O 2 将 Fe 2+ 氧化为 Fe 3+ :
,故 B 错误;
C . “84” 消毒液中含有 Cl - 和 ClO - ,在酸性条件下能发生归中反应生成氯气,向 “84” 消毒液中滴加足量的稀硫酸: ,故 C 正确;
D .向澄清石灰水中通入足量的 生成溶于水的碳酸氢钙,离子方程式为:
,故 D 错误;
故选 C 。
本卷还有30题,登录并加入会员即可免费使用哦~

该作品由: 用户柠檬分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。