二甲醚 (CH 3 OCH 3 ) 在制药、燃料、农药等化学工业中有许多独特的应用,同时因其能作为可再生的清洁能源而受到重视。
(1) 已知: ①CO(g)+2H 2 (g) CH 3 OH(g) △ H 1 =-90.1kJ·mol -1
②3CO(g)+3H 2 (g) CH 3 OCH 3 (g)+CO 2 (g) △ H 2 =-260.2kJ·mol -1
③CO(g)+H 2 O(g) CO 2 (g)+H 2 (g) △ H 3 =-41.6kJ·mol -1
则反应 2CH 3 OH(g) CH 3 OCH 3 (g)+H 2 O(g) △ H=___ 。
(2) 已知: 3CO(g)+3H 2 (g) CH 3 OCH 3 (g)+CO 2 (g) △ H 2 =-260.2kJ·mol -1 的反应速率与物质的量浓度之间的关系为 v 正 =k 正 c x (CO)•c x (H 2 ) , v 逆 =k 逆 c(CH 3 OCH 3 )•c(CO 2 ) , k 正 和 k 逆 是速率常数,只与温度有关。在 300℃ 时测得的相关数据如表所示。
| 实验编号 | 初始浓度 | 生成 CH 3 OCH 3 的初始速率 /(mol·L -1 ·s -1 ) | |
| c(CO)/(mol·L -1 ) | c(H 2 )/(mol·L -1 ) | ||
| 1 | 2.00×10 -3 | 2.00×10 -3 | 3.2×10 -3 |
| 2 | 1.00×10 -3 | 5.00×10 -3 | 2.0×10 -3 |
| 3 | 2.00×10 -3 | 3.00×10 -3 | 4.8×10 -3 |
①300℃ 时, k 正 的值为 ___ ;若 300℃ 时,初始浓度 c(CO)=c(H 2 )=3.00×10 -3 mol·L -1 ,则生成 CH 3 OCH 3 的初始速率为 ___mol·L -1 ·s -1 。升高温度后, k 正 、 k 逆 变化值较大的是 ___ 。
② 写出一种能提高容器中 CH 3 OCH 3 百分含量的措施: ____ 。
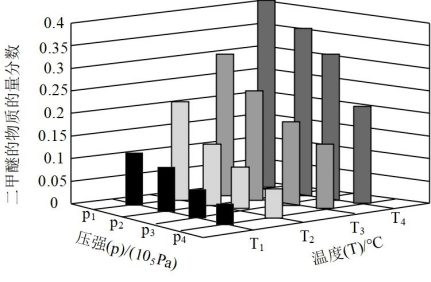
(3) 利用 CO 2 合成二甲醚反应: 2CO 2 (g)+6H 2 (g) CH 3 OCH 3 (g)+3H 2 O(g) △ H=-135.4kJ·mol -1 。某温度下,将 2.0molCO 2 和 6.0molH 2 充入 2L 密闭容器中,反应达平衡时,改变压强和温度,平衡体系中二甲醚的物质的量分数变化情况如图所示,则 p 1 ___( 填 “>”“<” 或 “=” ,下同 )p 2 。若 T 3 ℃ 、 p 3 ×10 5 Pa , T 4 ℃ 、 p 4 ×10 5 Pa 时,平衡常数分别为 K 3 、 K 4 ,则 K 3 ___K 4 。在
℃ 、 p 1 ×10 5 Pa 时, H 2 的平衡转化率为 ___%( 保留三位有效数字 ) 。
(4) 熔融碳酸盐燃料电池具有发电效率高、成本低等优点,某二甲醚碳酸盐燃料电池装置如图所示:
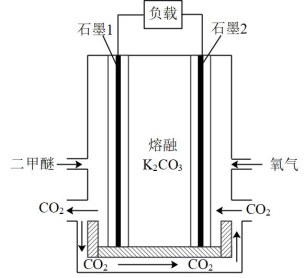
① 石墨 2 为 ___( 填 “ 正 ” 或 “ 负 ”) 极。
② 石墨 1 电极发生的电极反应式为 ___ 。
答案
(1)-38.4kJ·mol -1
(2) 4×10 5 1.08×10 -2 k 逆 适当降低温度或增大压强
(3) > < 57.1
(4) 正 CH 3 OCH 3 -12e - +6 =8CO 2 ↑+3H 2 O
【解析】
(1)
根据盖斯定律,反应 ②-2× 反应 ①- 反应 ③ 可得
;
(2)
① 由 300℃ 时测得的相关数据计算可知: 、
,
。若初始浓度
,则
。由于该反应为放热反应,升高温度后,平衡逆向移动,即升高温度,
增大得更多些。
② 该反应为气体分子数减小的放热反应,适当降低温度或增大压强均可使平衡正向移动,从而提高 的百分含量;
(3)
该反应为气体分子数减小的放热反应,故反应达到平衡后,二甲醚的物质的量分数随着温度的升高而减小,随压强增大而增大,该反应的平衡常数随温度的升高而减小。由题图可知,在相同温度 和
两种不同压强下,
下对应的二甲醚的物质的量分数较大,故
。在相同压强下,
℃ 和
℃ 两种不同温度下,
℃ 对应的二甲醚的物质的量分数较大,故
,由于化学平衡常数只与温度有关,该反应为放热反应,则
。在
℃ 、
下,设反应达平衡时
的物质的量浓度为
,则列出三段式:
由题图可知,此时二甲醚的物质的量分数为 ,解得
,故
的平衡转化率为
。
(4)
① 由图示可知,电池工作时,二甲醚失电子参与负极反应,氧气得电子参与正极反应,石墨 1 为负极,石墨 2 为正极;
② 石墨 1 电极反应式为 。
