能量通常包括热能、电能、光能、机械能、化学能等,下列有关能量转化关系的判断错误的是
A .充电电池:电能转化为化学能
B .干电池:化学能转化为电能
C .木炭燃烧:化学能转化为热能和光能
D .风力发电:风能转化为机械能,机械能转化为电能
A
【解析】
【详解】
A .充电电池:在充电时实现电能转化为化学能,放电时实现化学能转化为电能, A 错误;
B .干电池就是一次电池,只能实现化学能转化为电能, B 正确;
C .木炭燃烧是一个放热反应,故实现的是化学能转化为热能和光能, C 正确;
D .风力发电是将风能转化为风力发电机的机械能,机械能再转化为电能, D 正确;
故答案为: A 。
下列实验操作、现象和结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将碳酸氢钠与柠檬酸在烧杯中混合后搅拌 | 烧杯壁温度降低 | 该反应为吸热反应 |
| B | 用灼烧后的铂丝蘸取某溶液,放酒精灯上灼烧 | 火焰的颜色为黄色 | 该溶液一定含 K + |
| C | 将用砂纸打磨后的镁条放入沸水中 | 溶液变浑浊 | 镁失电子的能力强 |
| D | 将某固体化合物熔融后做导电性实验 | 电路中灯泡变亮 | 该化合物中一定含离子键 |
A . A B . B C . C D . D
B
【解析】
【详解】
A .烧杯壁温度降低,说明二者反应过程中吸收热量,导致周围环境温度降低, A 正确;
B .火焰的颜色为黄色说明含有 Na + ,钾离子的焰色试验要透过蓝色钴玻璃片进行观察,且为紫色, B 错误;
C .镁与沸水反应生成氢氧化镁和氢气,氢氧化镁为白色沉淀,溶液变浑浊,可以说明镁失电子的能力强, C 正确;
D .离子化合物在熔融状态或水溶液中导电,故该化合物中一定含有离子键, D 正确;
综上所述答案为 B 。
我国空间站将在 2022 年前后建成,为此,需要提前造好飞船,航天飞船可用腓 (N 2 H 4 ) 做动力源,已知: 1g 液态肼和足量的液态过氧化氢反应生成 N 2 和水蒸气时放出 20.05kJ 热量,化学方程式为: N 2 H 4 +2H 2 O 2 =N 2 ↑+4H 2 O 。下列说法中正确的是
A .该反应中过氧化氢做还原剂
B .肼 (N 2 H 4 ) 分子中只存在极性共价键
C .该反应的反应物总能量高于生成物的总能量
D .该反应过程中断开旧化学键吸收的能量大于形成新化学键释放的能量
C
【解析】
【详解】
A .该反应中,过氧化氢中氧元素化合价降低,过氧化氢做氧化剂,故 A 错误;
B .肼 (N 2 H 4 ) 分子中存在 N-H 和 N-N 键, N-H 是极性共价键、 N-N 是非极性共价键,故 B 错误;
C . N 2 H 4 +2H 2 O 2 =N 2 ↑+4H 2 O 反应放热,该反应的反应物总能量高于生成物的总能量,故 C 正确;
D . N 2 H 4 +2H 2 O 2 =N 2 ↑+4H 2 O 反应放热,该反应过程中断开旧化学键吸收的能量小于形成新化学键释放的能量,故 D 错误;
选 C 。
苯的亲电取代反应分两步进行,可表示为 E + + ![]()
![]()
![]() +H + ,生成中间体的一步是加成过程,中间体失去氢离子的
+H + ,生成中间体的一步是加成过程,中间体失去氢离子的 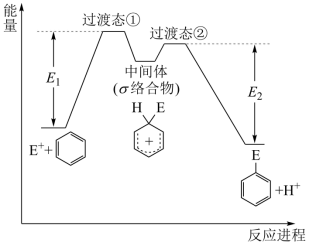 一步是消除过程,其机理亦称加成 — 消除机理,苯的亲电职代反应进程和能量的关系如图,下列说法错误的是
一步是消除过程,其机理亦称加成 — 消除机理,苯的亲电职代反应进程和能量的关系如图,下列说法错误的是
A .反应 Ⅰ 为苯亲电取代的决速步骤 B . E 1 与 E 2 的差值为总反应的焓变
C .中间体的能量比苯的高,稳定性比苯的差 D .反应过程中,环上碳原子的杂化类型发生了变化
B
【解析】
【详解】
A .反应需要活化能越大,反应越难,由图可知该反应的决速步骤反应为反应 Ⅰ ,故 A. 正确;
B .焓变与两步反应活化能的差值无关,与产物和反应物的能量差值有关,故 B 错误;
C .由图知中间体的能量比苯的高,稳定性比苯的差(能量越低越稳定),故 C 正确;
D .由图可知反应过程中中间体存在一个碳原子形成四个单键的中间状态反应过程中,环上此碳原子的杂化类型为 sp 3 杂化,苯环碳的杂化为 sp 2 反应过程中,环上碳原子的杂化类型发生了变化,故 D 正确;
故答案: B 。
氨是农业上 “ 氮的固定 ” 的必需原料,随着世界人口的增长,氨的需求量在不断增大。科研人员新发现以磷盐作质子 (H + ) 传导体,以四氢呋喃 ( 无色易挥发的液体 ) 为电解剂,利用电化学法将氮气还原成氨的原理如图所示。下列说法错误的是

A . M 电极为阳极,电极反应式为 H 2 -2e - =2H +
B . (Ⅰ)→(Ⅱ) 的变化中,磷原子的成键数目不发生变化
C .图示中最后一步反应为 3Li+N 2 +3H + =3Li + +2NH 3
D .该方法制备氨气所需的温度低于传统工业合成氨的温度
C
【解析】
【详解】
A .据图可知, M 电极上氢气被还原为氢离子,为阳极,电极反应式为 H 2 -2e - =2H + , A 正确;
B .据图可知 (Ⅰ)→(Ⅱ) 的变化中,磷原子都是形成 4 个共价键, B 正确;
C .最后一步反应中, Li + 先被还原为 Li 单质,然后将 N 2 还原为 NH 3 ,同时又生成 Li + ,所以 Li + 为催化剂,反应方程式为 N 2 +3H + 2NH 3 , C 错误;
D .该装置为电解装置,利用电能转化为化学能,即合成氨所需的能量大部分是由电能转化,则所需的热能较少,所需的温度较低, D 正确;
综上所述答案为 C 。
本卷还有28题,登录并加入会员即可免费使用哦~

该作品由: 用户李辉分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。