丙酮酸 (CH 3 COCOOH) 是一元弱酸。 298K 时,向 20mL0.1mol·L -1 丙酮酸溶液中滴加 pH=13 的 NaOH 溶液,溶液中 lg 与 pH 的关系曲线如图所示。下列说法错误的是
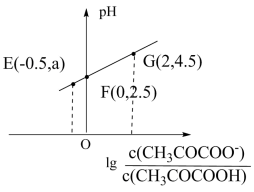
A . E 点溶液中, a=2
B . 298K 时, CH 3 COCOOH 的电离常数的数量级为 10 -3
C . G 点对应的 NaOH 溶液的体积为 20mL
D . E 、 F 、 G 三点对应的溶液中水的电离程度: E<F<G
答案
C
【解析】
【分析】
根据 F 点 lg =0 ,求出丙酮酸 (CH 3 COCOOH) K a ,再求出 E 点的 pH , G 点对应的 NaOH 溶液的体积如果为 20mL ,则刚好完全反应,溶质为 CH 3 COCOONa ,溶液应呈碱性,由此判断 C 、 D 的正误。
【详解】
A . E 点溶液中, lg =-0.5 ,
=10 -0.5 , Ka=
×c(H + )=10 -2.5 , c(H + )=10 -2 , pH=a=2 ,故 A 正确;
B . F 点 lg =0 ,则 c(
)=c(
HA) ,此时溶液 pH=2.5 ,即 c(H + )=10 -2.5 mol/L ,所以 K a=
×c(H + )=c(H + )=10 -2.5 =5.1×10 -3 , 298K 时, CH 3 COCOOH 的电离常数的数量级为 10 -3 ,故 B 正确;
C . G 点对应的 NaOH 溶液的体积如果为 20mL ,则刚好完全反应,溶质为 CH 3 COCOONa ,溶液应呈碱性,但 E 点 pH=4.5 ,呈酸性,故 C 错误;
D . E 、 F 、 G 三点随 NaOH 的加入 CH 3 COCOONa 的浓度越来越大, CH 3 COCOONa 水解促进水电解,对应的溶液中水的电离程度: E<F<G ,故 D 正确;
故选 C 。

