原电池电极的 “ 正 ” 与 “ 负 ” 不仅与电极材料的性质有关,也与电解质溶液有关 . 下列说法中不正确的是
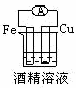
A .由 Fe 、 Cu 和 溶液组成的原电池中,负极反应式为:
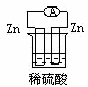
B .由 Zn 、 Cu 和稀硫酸组成的原电池中,负极反应式为:
C .由 Al 、 Mg 和 NaOH 溶液组成的原电池中,负极反应:
D .由 Al 、 Cu 和浓 溶液组成的原电池中,负极反应式为:
答案
D
【解析】
【详解】
A .由 Fe 、 Cu 和 溶液组成的原电池, Fe 和 Cu 都与
溶液反应,但 Fe 的金属性比 Cu 强,所以 Fe 失电子,作负极, Cu 作正极,所以负极反应式为:
,故 A 正确;
B .由于 Zn 和稀硫酸反应而失电子, Cu 和稀硫酸不反应,所以 Zn 作负极, Cu 作正极,负极反应式为: ,故 B 正确;
C .因 Al 和 NaOH 溶液反应而失去电子, Mg 和 NaOH 溶液不反应,所以 Al 作负极, Mg 作正极,负极反应为: ,故 C 正确;
D .由于 Al 和浓 发生钝化现象, Cu 和浓
能自发进行反应,所以 Cu 作负极, Al 作正极,负极反应式为:
,故 D 错误;
答案选 D 。



 B
B
 D
D