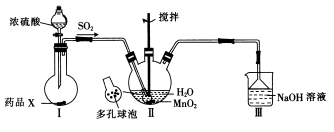
二氯化砜 (SO 2 Cl 2 ) 是一种重要的有机合成试剂,实验室可利用 SO 2 与 Cl 2 反应制取少量的 SO 2 Cl 2 。装置如图 ( 有些支持装置省略了 ) 所示。已知 SO 2 Cl 2 的熔点为 -54 . 1 ℃,沸点为 69 . 1 ℃;常温下比较稳定,受热易分解,遇水能发生剧烈的水解反应,产物之一为氯化氢气体。
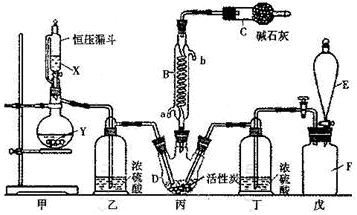
( 1 )仪器 E 的名称是 _______ ,由 B 的使用可知 SO 2 与氯气之间的反应居于 ______ ( 填 “ 放 ” 或 “ 吸 ”) 热反应, B 处反应管冷却水应从 ___________ ( 填 “a” 或 “b”) 接口通入。如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是 __________ 。
( 2 )试剂 X 、 Y 的组合最好是 _________ 。
a . 98% 硫酸和铜 b .稀硝酸和亚硫酸钠固体 c . 60% 硫酸和亚硫酸钾固体
( 3 )戊是贮气装置,则 E 中的试剂是 _________ ;若缺少装置乙和丁,潮湿的氯气和二氧化硫之间发生反应的化学方程式是 ___________________________ .
( 4 )取 1 . 00g 蒸馏后的液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为 1 . 50g ,则所得馏分中二氯化砜的质量百分含量为 __________ %( 结果保留小数点后 1 位 ) 。
( 5 )二氯化砜应储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是 ______ 。
答案
分液漏斗 放 a 该反应是放热反应,降低温度能使平衡正向移动,有利于二氯化砜的生成 c 饱和食盐水 SO 2 + Cl 2 +2H 2 O=H 2 SO 4 +2HCl 86.9 因为 SO 2 Cl 2 自身分解生成 Cl 2 , Cl 2 溶于使液体呈黄色
【详解】
( 1 )根据装置图可知, E 为分液漏斗,因蛇形冷凝管的作用是冷凝回流而反应又没有加热,故 SO 2 与氯气间的反应为放热反应;根据下进上出,的原则, B 处反应管冷却水应从 a 接口通入;由于该反应是放热反应,降低温度能使平衡正向移动,有利于二氯化砜的生成;故答案为分液漏斗;放; a ;该反应是放热反应,降低温度能使平衡正向移动,有利于二氯化砜的生成;
( 2 )甲是制备 SO 2 的装置,铜与浓硫酸反应需要加热,硝酸能氧化 SO 2 ,所以用 c . 60% H 2 SO 4 +K 2 SO 3 来制备 SO 2 ,故选 c ;
( 3 )因氯水不溶于饱和食盐水,故 E 中的试剂是饱和食盐水,氯气在水存在的条件下可将 SO 2 氧化成硫酸,自身被还原为 HCl ,反应的方程式为 SO 2 +Cl 2 +2H 2 O=H 2 SO 4 +2HCl ,故答案为饱和食盐水; SO 2 +Cl 2 +2H 2 O=H 2 SO 4 +2HCl ;
( 4 )设所得馏分中二氯化砜的质量百分含量为 x ,则:
SO 2 Cl 2 ~ H 2 SO 4 ~ BaSO 4
135 233
1.00g×x 1.5g
所以 135 : 233=1.00g×x : 1.5g
解得 x=86.9%
故答案为 86.9 ;
( 5 ) SO 2 Cl 2 久置后分解会生成氯气,可能是溶解氯气所致,故答案为二氯化砜久置后分解生成的氯气,溶解在二氯化砜中,使液体呈黄色。