高铁酸钠 (Na 2 FeO 4 ) 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用化学方程式表示为: 3NaClO + 2Fe(OH) 3 + 4NaOH = 2Na 2 FeO 4 + 3NaCl + 5H 2 O
(1) 请用双线桥表示该氧化还原反应中电子转移的方向和数目 _______ ;
(2) 该反应中氧化剂是 _______ ;氧化产物是 _______ ;
(3) 反应中当有 3mol 电子转移时,生成高铁酸钠的质量为 _______ g ;
(4) 将高铁酸钠溶液滴入稀硫酸中,会放出 O 2 ,并生成 Na 2 SO 4 和 Fe 2 (SO 4 ) 3 ,请写出并配平化学方程式 _______ 。
答案
 NaClO Na 2 FeO 4 166 4Na 2 FeO 4 +10H 2 SO 4 =4Na 2 SO 4 +2Fe 2 (SO 4 ) 3 +3O 2 ↑+10H 2 O
NaClO Na 2 FeO 4 166 4Na 2 FeO 4 +10H 2 SO 4 =4Na 2 SO 4 +2Fe 2 (SO 4 ) 3 +3O 2 ↑+10H 2 O
【分析】
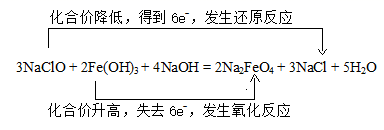
3NaClO + 2Fe(OH) 3 + 4NaOH = 2Na 2 FeO 4 + 3NaCl + 5H 2 O 反应中, NaClO 中氯元素由 +1 价降低到 NaCl 中的 -1 价,发生了还原反应, NaClO 做氧化剂, 3NaClO 完全被还原,转移 6mol 电子; Fe(OH) 3 中铁元素由 +3 价升高到 Na 2 FeO 4 中 +6 价,发生了氧化反应, Fe(OH) 3 做还原剂, Na 2 FeO 4 为氧化产物。
【详解】
(1) 结合以上分析可知,该反应发生后,转移 6mol 电子,用双线桥表示该氧化还原反应中电子转移的方向和数目: 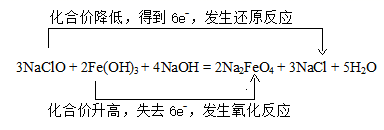 ;
;
(2) 结合以上分析可知,该反应中氧化剂是 NaClO ,氧化产物是 Na 2 FeO 4 ;
(3) 根据问题 (1) 可知, 6e - ~ 2Na 2 FeO 4 ,所以反应中当有 3mol 电子转移时,生成高铁酸钠的物质的量为 1mol ,质量为 1mol×166g/mol=166g ;
(4) 将高铁酸钠溶液滴入稀硫酸中,会放出 O 2 ,并生成 Na 2 SO 4 和 Fe 2 (SO 4 ) 3 ,反应的表达式为: Na 2 FeO 4 +H 2 SO 4 →Na 2 SO 4 +Fe 2 (SO 4 ) 3 +O 2 ↑+H 2 O ,铁元素由 +6 价降低到 +3 价,所以 2Na 2 FeO 4 →Fe 2 (SO 4 ) 3 ,化合价共降了 6 价;氧元素由 -2 价升高到 0 价,化合价升高了 4 价,根据化合价升降总数相等规律, Na 2 FeO 4 填系数 4 , Fe 2 (SO 4 ) 3 填系数 2 , O 2 填系数 3 ,据原子守恒规律配平其它物质的系数,配平后的方程式为: 4Na 2 FeO 4 +10H 2 SO 4 =4Na 2 SO 4 +2Fe 2 (SO 4 ) 3 +3O 2 ↑+10H 2 O 。



