Ⅰ. 如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为:
CH 3 CH 2 OH CH 2 =CH 2 ↑ + H 2 O ,回答下列问题:

( 1 )图 1 中仪器 ① 、 ② 的名称分别为 ________ 、 ________ 。
( 2 )收集乙烯气体最好的方法是 ________ 。
( 3 )向溴的四氯化碳溶液中通入乙烯 ( 如图 2) ,溶液的颜色很快褪去,该反应属于 ____ ( 填反应类型 ) 。
Ⅱ. 实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:
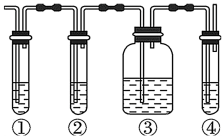
( 1 )图中 ① 、 ② 、 ③ 、 ④ 装置盛放的试剂是下列中的 ( 将正确选项填入空格内 ) :
① __________ ; ② __________ ; ③ __________ ; ④ __________ 。
| A .品红溶液 | B .氢氧化钠溶液 |
| C .浓硫酸 | D .酸性高锰酸钾溶液 |
( 2 )能说明二氧化硫气体存在的现象是 ____________________ 。
( 3 )使用装置 ② 的目的是 ________________________________ 。
( 4 )使用装置 ③ 的目的是 _______________________________ 。
( 5 )验证含有乙烯的现象是 ________________________________ 。
答案
温度计 圆底烧瓶 排水法 加成反应 A B A D ① 中品红溶液褪色 吸收 SO 2 检验 SO 2 是否被除尽 ③ 中品红溶液不褪色, ④ 中 KMnO 4 溶液褪色
【详解】
Ⅰ. ( 1 )图 1 中仪器 ① 用于测量反应温度,名称为温度计;仪器 ② 由于盛放乙醇和浓硫酸的混合液,名称为圆底烧瓶;
( 2 )乙烯的密度与空气密度接近,不能使用排空气法收集,乙烯不溶于水,可以用排水法水解乙烯;
( 3 )向溴的四氯化碳溶液中通入乙烯(如图 2 ),乙烯与溴发生加成反应生成 1 , 2- 二溴乙烷,所以溶液的颜色很快褪去。
Ⅱ. ( 1 )装置 ① 中盛有品红溶液,用来检验二氧化硫的存在;然后将气体通入盛有氢氧化钠溶液的 ② 除去二氧化硫,再通入盛有品红溶液的 ③ 确定二氧化硫是否除干净,最后通入盛有酸性高锰酸钾的 ④ 检验乙烯的存在;故答案为 A ; B ; A ; D ;
( 2 )二氧化硫具有漂白性,能够使品红溶液褪色;
( 3 )装置 ② 用来除去 SO 2 气体,以免干扰乙烯的性质实验;
( 4 )装置 ③ 检验 SO 2 是否被除尽,防止干扰乙烯的性质实验;
( 5 )装置 ③ 中的品红溶液不退色可以排除二氧化硫的干扰,若装置 ④ 中的酸性 KMnO 4 溶液退色,可证明乙烯的存在。



 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O 

