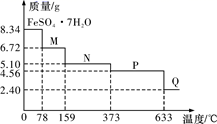
四氯化锡 (SnCl 4 )是合成有机锡化合物的原料,其熔点为-33℃,沸点为114℃,在潮湿的空气中强烈水解产生有刺激性的白色烟雾,产物之一为SnO 2 。实验室制备四氯化锡的操作是:将金属锡熔融,然后泼入冷水,制成锡花;将干燥的锡花加入反应器中,再向反应器中缓慢地通入干燥的氯气。 (装置C中的试剂Ⅹ未画出)
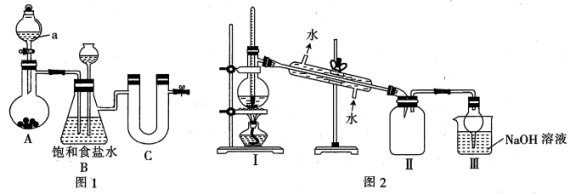
I.图1为实验室制备干燥氯气的实验装置(夹持装置已略)
(1)该装置制备氯气选用的药品为漂粉精固体[主要成分Ca(ClO 2 ]和浓盐酸,A中发生反应的化学方程式为 _________________________________ 。
(2)装置B中的饱和食盐水能够除去Cl 2 中的 HCl,此外还有 ___________ 作用。
(3)试剂Ⅹ可能为 ___________ (填标号)。
A.无水氯化钙 B.浓硫酸 C.五氧化二磷 D.碱石灰
(4)用锡花代替锡粒的目的是 _________________________________ 。
(5)四氯化锡在潮湿空气中水解的化学方程式为 _________________________________ 。
Ⅱ.图2是蒸馏SnCl 4 的装置
(6)该装置尚有两处不当之处,它们分别是 ____________________ 、 ______________________ 。
(7)实验用的锡花中含有金属铜。某同学设计下列实验测定锡花的纯度:
第一步:称取 7.500g锡花溶于足量稀硫酸中,充分反应后过滤;
第二步:向滤液中加入过量 Fe 2 (SO 4 ) 3 ,将生成的 Sn 2+ 氧化成 Sn 4+ ;
第三步:用 0.9500mol·L - 1 的 K 2 Cr 2 O 7 溶液滴定生成的 Fe 2+ ,发生反应的方程式为 Fe 2+ +Cr 2 O 7 2- +H + →Cr 3+ +Fe 3+ +H 2 O(未配平)
若达到滴定终点时共消耗 21.00mLK 2 Cr 2 O 7 溶液,试计算锡花中锡的百分含量: ___________ (结果保留4位有效数字)。
答案
Ca(ClO) 2 +4HCl(浓)=CaCl 2 +2Cl 2 ↑+2H 2 O 安全瓶 AC 增大与氯气的接触面积,加快反应速率 SnCl 4 +2H 2 O=SnO 2 +4HCl 温度计水银球位置不对 Ⅱ和Ⅲ之间缺少干燥装置; 94.96%
【详解】
(1)图I装置制备氯气选用的药品为漂粉精固体[主要成分Ca(ClO 2 ]和浓盐酸反应生成氯化钙、氯气与水,A中发生反应的化学方程式为Ca(ClO) 2 +4HCl(浓)=CaCl 2 +2Cl 2 ↑+2H 2 O。答案:Ca(ClO) 2 +4HCl(浓)=CaCl 2 +2Cl 2 ↑+2H 2 O。
( 2)制备的氯气中含有HCl,饱和食盐水除去Cl 2 中的 HCl;若C中发生堵塞,装置内气压增大,B中长颈漏斗中液面上升,形成水柱,所以B还起到了安全瓶的作用。故答案为安全瓶;
(3) 四氯化锡极易水解,通入的氯气应干燥,U形管中试剂X干燥氯气,不能为碱性干燥剂,碱性干燥剂可以吸收氯气;不能为液体干燥剂,否则气体不能通过,可以选择氯化钙、五氧化二磷,故答案为AC;
(4)用锡花代替锡粒的目的是:增大与氯气的接触面积,加快反应速率。故答案为增大与氯气的接触面积,加快反应速率;
(5) 四氯化锡遇水强烈水解,根据水解原理可知,应生成Sn(OH) 4 、 HCl,产物之一是固态二氧化锡,说明Sn(OH) 4 分解生成 SnO 2 与 H 2 O,故水解生成SnO 2 、 HCl,反应方程式为:SnCl 4 +2H 2 O=SnO 2 +4HCl。故答案为SnCl 4 +2H 2 O=SnO 2 +4HCl;
(6)温度计水银球位置不对,应再蒸馏烧瓶支管口处;四氯化锡遇水强烈水解,而装置Ⅲ中的水蒸气易进入Ⅱ中,使其发生水解,二者之间缺少干燥装置;故答案为温度计水银球位置不对;Ⅱ和Ⅲ之间缺少干燥装置;
( 7)第二步:过量Fe 2 (SO 4 ) 3 ,将 Sn 2+ 氧化成 Sn 4+ ,本身被还原为亚铁离子,反应的离子方程式为: 2Fe 3+ +Sn 2+ =2Fe 2+ +Sn 4+ ,反应中消耗的 K 2 Cr 2 O 7 的物质的量为 0.9500mol/L×0.021L=0.01995mol,6Fe 2+ +Cr 2 O 7 2- +14H + =2Cr 3+ +6Fe 3+ +7H 2 O。根据方程式可得关系式3Sn~3Sn 2+ ~ 3Fe 2 (SO 4 ) 3 ~ 6Fe 3+ ~ K 2 Cr 2 O 7 ,故 n(Sn)=3n(K 2 Cr 2 O 7) =3×0.01995mol=0.05985mol, Sn的质量为:0.05985mol×119g/mol=7.122g,试样中Sn的百分含量为=7.12g/7.500×100%=94.96%。因此,本题正确答案是:94.96%。



 N2+3Cu+3H2O
N2+3Cu+3H2O