现有下列短周期元素性质的有关数据:
| 元素编号 | a | b | c | d | e | f | g | h |
| 原子半径 /nm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最底 | | | | | | | | |
(1) 根据元素周期律确定 a 至 h8 种元素在周期表中的位置,将它们的元素编号填入下表相应的空格内 _______ 。
| | Ⅰ族 | Ⅱ族 | Ⅲ族 | Ⅳ族 | Ⅴ族 | Ⅵ族 | Ⅶ族 | Ⅷ族 |
| 第一周期 | | | | | | | | |
| 第二周期 | | | | | | | | |
| 第三周期 | | | | | | | | |
(2) 上述元素形成的常见氢化物中,分子间存在氢键的有 ( 填氢化物的化学式 ) _______ 。
(3) 氢化铝锂 ( ) 是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在 125 ℃时氢化铝锂分解为氢气、金属铝及氢化锂 (LiH) 。与氢化铝锂性质相似但较为温和的还原剂由上述 a 、 d 、 h 三种元素组成,请画出这种还原剂的电子式 _______ 。写出该物质受热分解的反应方程式 _______ 。
(4) 在元素周期表中,相邻近的元素在结构和性质上有许多相似之处。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除 外,还有
;碳元素的氢化物除
外,还有
等;与之相似的氮元素的氢化物除
外,还有 _______ ( 填化学式 ) ,其沸点比液氨 _______ ( 填 “ 高 ” 或 “ 低 ”) ,稳定性比氨 _______ ( 填 “ 好 ” 或 “ 差 ”) ,该氢化物与足量盐酸反应的化学方程式为 _______ 。
答案
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | a | |||||||
| 2 | g | | d | | c | | b | |
| 3 | h | | f | | | e | | |
、
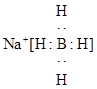
高 差
【解析】
【详解】
根据表中数据分析, agh 都为 +1 价,且 a 半径最小,所以 a 为氢元素,在第一周期族, g 为锂, h 为钠,分别为第二周族,和第三周期族。 B 为 -1 价,为氟元素, c 为 -3 价,半径比氟稍大,为氮元素, df 都为 +3 价,分别为硼和铝, e 为 -2 价,半径比氮原子半径大,应为硫。即 a 为氢, b 为氟, c 为氮, d 为硼, e 为硫, f 为铝, g 为锂, h 为钠,据此在周期表相应位置标志。如图:
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | a | |||||||
| 2 | g | | d | | c | | b | |
| 3 | h | | f | | | e | | |
(2) 上述元素形成的常见氢化物中,氮元素和氟元素的氢化物分子间存在氢键 、
。
(3) 硼和铝位于对角线,性质相似,所以有氢、硼和钠形成的还原剂的电子式为 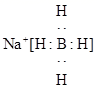 ,其受热分解的反应方程式
,其受热分解的反应方程式 。
(4) 在元素周期表中,相邻近的元素在结构和性质上有许多相似之处。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除 外,还有
;碳元素的氢化物除
外,还有
等;与之相似的氮元素的氢化物除
外,还有
,其相对分子质量比氨气大,所以沸点比液氨高,根据过氧化氢比水稳定性差分析,肼的稳定性比氨差,该氢化物与足量盐酸反应的化学方程式为
。
