海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。从海水中提取淡水和一些重要的化工产品的工艺流程如图所示。
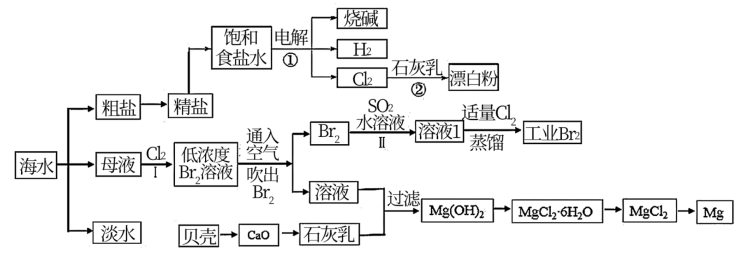
根据上述流程图回答下列问题:
(1) 写出反应 ①的化学反应方程式 _______ 。
(2) 工业上完成 常用的冶炼方法 _______ 。
(3) 通入热空气或水蒸气吹出 ,利用了溴的 _______ ( 填序号 ) 。
A .氧化性 B .还原性 C .挥发性 D .腐蚀性
(4) 写出步骤 Ⅱ 反应的离子方程式 _______ 。
(5) 从海水中获得淡水的主要方法有电渗析法、离子交换法和 _______ ( 填一种 ) 。
(6) 实验室模拟海水蒸馏法制取淡水,蒸馏过程中不可能用到的仪器有 _______ ( 填序号 ) 。
A .圆底烧瓶 B .容量瓶 C .直形冷凝管 D .接收器
(7) 离子交换法净化水的过程如图所示。下列说法正确的是 _______ ( 填序号 ) 。
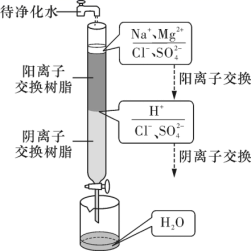
A .经过阳离子交换树脂后,水中阳离子总数减少
B .通过阴离子交换树脂后,水中只有 被除去
C .通过净化处理后的水,导电性增强
D .阴离子交换树脂填充段存在反应:
答案
电解 C
蒸馏法 B D
【分析】
根据上述工艺流程图分析,海水通过海水晒盐、海水淡化得到淡水和氯化钠溶液,得到饱和食盐水通电得到氢氧化钠、氢气和氯气,氯气通入石灰乳中得到氯化钙、次氯酸钙和水得到漂白粉,海水用硫酸酸化,加入适量的氯气,得到低浓度的溴溶液,用二氧化硫吸收得到溴离子,再通过通入氯气氧化溴离子生成溴单质,过程中富集溴,得到粗溴和硫酸。
【详解】
(1) 反应 ①电解饱和食盐水,化学反应方程式 。故答案为:
;
(2) 镁是活泼金属,工业上完成 常用的冶炼方法电解。故答案为:电解;
(3) 溴易挥发,通入热空气或水蒸气吹出 Br 2 ,利用了溴的挥发性,故选 C ;故答案为: C ;
(4) 步骤 Ⅱ 反应溴与二氧化硫反应生成硫酸和氢溴酸,离子方程式 。故答案为:
;
(5) 从海水中获得淡水的主要方法有电渗析法、离子交换法和蒸馏法 ( 填一种 ) 。故答案为:蒸馏法;
(6) 蒸馏操作可能使用蒸馏烧瓶、直形冷凝管、接收器等,不会使用容量瓶,故答案为: B ;
(7)A .离子交换时,按电荷守恒进行,经过阳离子交换树脂后, 1 个 Mg 2+ 被 2 个 H + 替换,所以水中阳离子总数增多, A 错误;
B .通过阴离子交换树脂后,水中 Cl - 、 都被除去, B 错误;
C .通过净化处理后的水,离子浓度大大减小,导电性减弱, C 错误;
D .阴离子交换树脂填充段生成 OH - ,与阳离子交换树脂段生成的 H + 结合,存在反应 H + +OH - =H 2 O , D 正确;
故答案为: D 。


