下列有关化学用语表述不正确的是
A . 的结构示意图:
 B . 中子数为 9 的氧原子: 9 O
B . 中子数为 9 的氧原子: 9 O
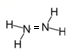
C . N 2 H 4 的结构式: ![]() D . 氮化镁的电子式为:
D . 氮化镁的电子式为: ![]()
答案
B
【详解】
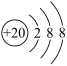
A .钙的核电荷数为 20 , 的结构示意图
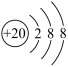 ,故 A 正确;
,故 A 正确;
B .元素符号左上角的数字表示质量数,质量数=中子数+质子数,所以中子数为 9 的氧原子: O ,故 B 错误;
C . N 2 H 4 分子中 4 个氢原子与 2 个氮原子形成四个共价键,两个氮原子之间形成一条共价键,所以 N 2 H 4 的结构式: ![]() ,故 C 正确;
,故 C 正确;
D .氮化镁属于离子化合物,镁失去最外层电子,氮原子得到电子,所以氮化镁的电子式为: ![]() ,故 D 正确;
,故 D 正确;
故答案: B 。


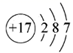 D
D