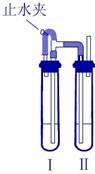
为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。

(1) 往 A 、 B 溶液中分别滴入几滴 KSCN 溶液,溶液的颜色: A _______ , B _______ 。
(2) 写出上述过程中有关反应的离子方程式:
Fe 2 O 3 →A _______ ;
A→B _______ 。
(3)B→C 可看到的现象是 _______ 。
(4) 将 A 的饱和溶液滴入沸水中并不断加热,可制得 _______ 胶体;当光束通过该胶体时,可看到一条光亮的 “ 通路 ” ,这种现象称为 _______ 。
答案
血红色 不变色 Fe 2 O 3 +6 H + = 2Fe 3+ +3H 2 O 2Fe 3+ +Fe=3Fe 2+ 由白色絮状沉淀迅速变成灰绿色,最后变成红褐色 Fe(OH) 3 丁达尔效应
【分析】
由题给实验流程可知,向 Fe 2 O 3 固体中加入稀盐酸,发生的反应为 Fe 2 O 3 与稀盐酸反应生成氯化铁和水,向氯化铁溶液中加入过量铁粉发生的反应为氯化铁溶液与铁反应生成氯化亚铁,向氯化亚铁溶液中加入氢氧化钠溶液发生的反应为氯化亚铁溶与氢氧化钠溶液立即反应生成氢氧化亚铁白色沉淀和氯化钠,氢氧化亚铁白色沉淀被空气中氧气氧化为氢氧化铁,沉淀迅速变为灰绿色,最终变为红褐色。
【详解】
(1) 由分析可知, A 溶液为氯化铁溶液,向氯化铁溶液中滴入硫氰化钾溶液,氯化铁溶液与硫氰化钾溶液反应生成硫氰化铁,溶液变为血红色, B 溶液为氯化亚铁溶液,向氯化亚铁溶液滴入硫氰化钾溶液,氯化亚铁溶液与硫氰化钾溶液不反应,溶液的颜色没有变化,故答案为:血红色;不变色;
(2) Fe 2 O 3 →A 发生的反应为 Fe 2 O 3 与稀盐酸反应生成氯化铁和水,反应的离子方程式为 Fe 2 O 3 +6 H + = 2Fe 3+ +3H 2 O ; A→B 发生的反应为氯化铁溶液与铁反应生成氯化亚铁,反应的离子方程式 Fe 3+ +Fe=3Fe 2+ ,故答案为: Fe 2 O 3 +6 H + = 2Fe 3+ +3H 2 O ; Fe 3+ +Fe=3Fe 2+ ;
(3) B→C 发生的反应为氯化亚铁溶与氢氧化钠溶液立即反应生成氢氧化亚铁白色沉淀和氯化钠,氢氧化亚铁白色沉淀被空气中氧气氧化为氢氧化铁,沉淀迅速变为灰绿色,最终变为红褐色,故答案为:立即生成白色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色;
(4) 将氯化铁的饱和溶液滴入沸水中并不断加热,可制得氢氧化铁胶体,当光束通过氢氧化铁胶体时,可看到一条光亮的 “ 通路 ” ,这种现象称为丁达尔效应,故答案为: Fe(OH) 3 ;丁达尔效应。