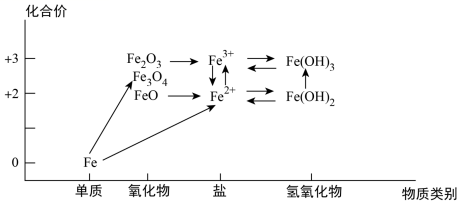
铁及其化合物的 “ 价类二维图 ” 如图。回答下列问题:
(1) 预测 既有氧化性又有还原性,其依据是 _______
(2) 检验溶液中的 ,常用的试剂是 _______ 。
(3) 氧化铁和铝粉可用于野外焊接钢轨,用化学方程式表示反应原理 _______ 。
(4) 向 溶液中滴加氯水,反应的离子方程式 _______ 。如果反应后的溶液中还有
存在,选用 _______ 试剂,产生 _______ 现象证明其存在。
答案
化合价为 +2 ,为中间价,既能升高又能降低 KSCN 溶液 2Al+Fe 2 O 3
Al 2 O 3 +2Fe 2Fe 2+ +Cl 2 =2Fe 3+ +2Cl - 铁氰化钾 蓝色沉淀
【分析】
根据铁盐和亚铁盐的性质和检验方法分析解答。
【详解】
(1)Fe 2+ 的化合价为 +2 ,可以升高也可以降低,所以既有氧化性又有还原性,故答案为: Fe 2+ 的化合价为 +2 ,为中间价,既能升高又能降低;
(2)Fe 3+ 与 KSCN 溶液显血红色,所以检验溶液中的 Fe 3+ ,常用的试剂是 KSCN 溶液,故答案为: KSCN 溶液;
(3) 氧化铁和铝粉在高温下反应生成铁和氧化铝,反应的化学方程式为 2Al+Fe 2 O 3 2Fe+Al 2 O 3 ,故答案为: 2Al+Fe 2 O 3
2Fe+Al 2 O 3 ;
(4) 氯气与 FeCl 2 反应生成氯化铁,反应的离子方程式为 2Fe 2+ +Cl 2 =2Fe 3+ +2Cl - ,如果反应后的溶液中还有 Fe 2+ 存在,可以选用铁氰化钾试剂,如果产生蓝色沉淀,即可证明其存在,故答案为: 2Fe 2+ +Cl 2 =2Fe 3+ +2Cl - ;铁氰化钾;蓝色沉淀。