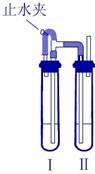
兴趣小组分析了用硫铁矿烧渣 ( 主要成份 Fe 2 O 3 、 Fe 3 O 4 、 FeO 等 ) 制备铁红 (Fe 2 O 3 ) 的流程图并进行了铁红性质实验。
( 一 ) 铁红制备的流程图分析:
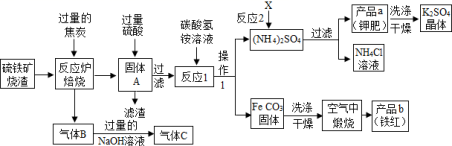
(1) 实验室完成操作 1 ,用到的玻璃仪器有烧杯、玻璃棒和 ___________ ( 填仪器名称 ) 。
(2) 你认为对气体 C 最佳的处理方法是 ___________ ( 填选项序号 ) 。
A .冷却后排入空气 B .燃烧后排放 C .再通入反应炉
(3) 反应 1 的反应温度一般需控制在 35 ℃以下,其目的是 ___________ 。
(4) 若焙烧中碳与四氧化三铁反应后 B 中气体的比例恰好是 1 ∶ 1 ,其化学方程式: ___________ 。
(5) 反应 2 中相关物质的溶解度如表,你认为该反应在常温下能实现的原因是: ___________ 。
| 物质 | X | K 2 SO 4 | NH 4 C1 | (NH 4 ) 2 SO 4 |
| 溶解度 g(25 ℃ ) | 34.0 | 11.1 | 37.2 | 19.2 |
为检验硫酸钾晶体是否洗涤干净,可取最后一次洗涤液,先加入 ___________ ,振荡、静置,再向上层清液中滴加 ___________ ,观察现象即可判断。
A .硝酸银溶液 B .过量的氯化钡溶液 C .过量的硝酸钡溶液
( 二 ) 铁红的性质实验
(6) 实验装置:已知:草酸晶体 (H 2 C 2 O 4 ·3H 2 O) 在浓 H 2 SO 4 作用下受热分解,化学方程式为 H 2 C 2 O 4 ·3H 2 O CO 2 ↑ + CO↑ + 4H 2 O
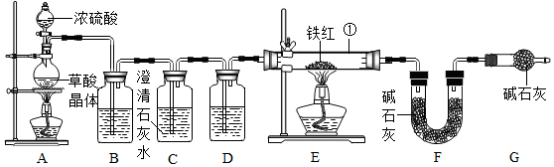
①实验前应先 ___________ 。
②进入 E 中的气体是纯净、干燥的一氧化碳,则 B 、 D 中的试剂依次是 ___________ 、 ___________ ( 填字母编号 ) 。
A .浓硫酸 B .澄清石灰水 C .氢氧化钠溶液
③ C 装置的作用是 ___________ 。
答案
漏斗 C 防止碳酸氢铵受热分解 9Fe 3 O 4 +8C 9Fe+4CO 2 ↑+4CO↑ 常温下 K 2 SO 4 的溶解度小 C A 检查装置的气密性 C A 检验二氧化碳是否被除尽
【分析】
根据铁红制备的流程图,反应炉中过量的焦炭还原氧化铁生成铁和二氧化碳,过量的一氧化碳会随二氧化碳逸出,因此气体 B 为一氧化碳和二氧化碳的混合气体,气体 B 通过足量的氢氧化钠溶液后,二氧化碳与氢氧化钠反应生成碳酸钠和水,因此气体 C 中主要含有一氧化碳,一氧化碳可作为还原剂重复利用;固体 A 为单质铁,和硫酸反应生成硫酸亚铁,过滤除去不反应的杂质,硫酸亚铁再和碳酸氢铵反应,生成碳酸铁沉淀和硫酸铵溶液,碳酸铁通过洗涤、干燥、煅烧生成氧化铁;硫酸铵溶液中加入 X ,得到氯化铵溶液和硫酸钾固体, X 为氯化钾,硫酸钾固体经过洗涤、干燥得到纯净的 K 2 SO 4 晶体;根据铁红的性质实验装置,浓硫酸与草酸反应生成 CO 2 和 CO 气体,二氧化碳一般用氢氧化钠溶液吸收,用澄清的石灰水可以检验二氧化碳是否除尽,干燥后在 E 中与铁红反应生成铁和二氧化碳, F 中的碱石灰可以吸收生成的二氧化碳, G 中碱石灰可以防止外界空气中的水蒸气和二氧化碳进入装置 F ,据此分析解答。
【详解】
( 一 )(1) 把不溶于液体的固体和液体分离的方法是过滤,过滤用到的玻璃仪器有:烧杯、玻璃棒、漏斗,故答案为:漏斗;
(2) 气体 C 主要成分是一氧化碳,一氧化碳可作为还原剂重复利用,对气体 C 最佳的处理方法是再通入反应炉中重复利用,故答案为: C ;
(3) 碳酸氢铵受热容易分解为氨气、水、二氧化碳,所以反应 1 的反应温度一般需控制在 35 ℃以下,故答案为:防止碳酸氢铵受热分解;
(4)C 与 Fe 3 O 4 在高温的条件下生成铁、二氧化碳和一氧化碳,其中一氧化碳和二氧化碳的比例恰好是 1 ∶ 1 ,反应的化学方程式为 9Fe 3 O 4 +8C 9Fe+4CO 2 ↑+4CO↑ ,故答案为: 9Fe 3 O 4 +8C
9Fe+4CO 2 ↑+4CO↑ ;
(5) 根据复分解反应发生的条件,反应 2 中没有不溶物,但常温下硫酸钾的溶解度较小,在生成物中可以以沉淀的形式出现,所以反应可以发生; K 2 SO 4 晶体表面可能吸附有少量氯化铵,为检验 K 2 SO 4 晶体是否洗涤干净,就是检验是否有氯化钾,可取最后一次洗涤液,此时是硫酸钾的溶液,可能含有氯化钾,而检验氯化钾是需要用硝酸银的,但是由于硫酸钾遇到硝酸银也会生成白色沉淀,所以应该先除去硫酸根离子的干扰,应该先加入过量的硝酸钡 ( 不能使用氯化钡,防止引入氯离子干扰后期的检验 ) 溶液,振荡、静置,再向上层清液中滴加硝酸银溶液,故答案为:常温下 K 2 SO 4 的溶解度小; C ; A ;
( 二 )(6) ①实验中有气体参与反应,因此实验前应先检查装置的气密性,否则会由于漏气使实验失败,故答案为:检查装置的气密性;
②根据方程式 H 2 C 2 O 4 ·3H 2 O CO 2 ↑ + CO↑ + 4H 2 O 可知,从 A 中出来的气体中含有一氧化碳和二氧化碳,二氧化碳一般用氢氧化钠溶液吸收,用澄清的石灰水可以检验二氧化碳是否除尽,一氧化碳可以用浓硫酸干燥;所以 B 中盛放的是氢氧化钠溶液,吸收二氧化碳,氢氧化钙是验证二氧化碳是否被除净, D 中盛放的是浓硫酸,干燥一氧化碳,故答案为: C ; A ;
③ F 中的碱石灰可以吸收生成的二氧化碳, G 中碱石灰可以防止外界空气中的水蒸气和二氧化碳进入装置 F ,因此进入 E 装置的气体中不能含有二氧化碳,澄清的石灰水是检验二氧化碳是否除尽,故答案为:检验二氧化碳是否被除尽。