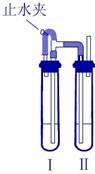
已知三氯化铁的熔点为 306 ℃,沸点为 315 ℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验:
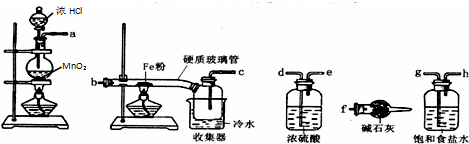
(1) 装碱石灰的仪器是 _______ ( 填仪器名称 ) 。
(2) 饱和食盐水的作用 _______ 。
(3) 反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油 ( 反应过程中不振荡 ) ,充分反应后,进行如下实验:
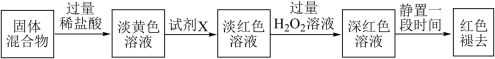
已知红色褪去的同时有气体生成,经检验为 O 2 。该小组内的同学们对红色褪去的原因提出了三种假设。
假设 I : H 2 O 2 还原 Fe 3+ ,使其转变为 Fe 2+ ;
假设 II : H 2 O 2 分解生成 O 2 , O 2 氧化试剂 X ;
假设 III : _______ ( 如果表达中遇到试剂 X ,请写出其化学式 ) 。
并对假设进行了以下实验研究:
①取褪色后溶液三份,第一份滴加 FeCl 3 溶液无明显变化;第二份滴加试剂 X ,溶液出现红色;第三份滴加稀盐酸和 BaCl 2 溶液,产生白色沉淀。
②另取同浓度的 FeCl 3 溶液滴加 2 滴试剂 X ,溶液变红,再通入 O 2 ,无明显变化。实验 ①说明假设 _______ 不正确;实验 ②的目的是 _______ ;由实验 ①②得出假设 _______ 是正确的。
答案
干燥管或球形干燥管 除去多氯气中的氯化氢气体 H 2 O 2 氧化 KSCN I 证明假设 II 不成立 III
【分析】
根据实验目的,首先制备氯气,制备的氯气中含有 HCl 和水蒸气, HCl 和水蒸气影响后续实验,因此必须除去,即 a→g→h→d→e ,得到纯净的氯气,与铁粉反应,即 e→b→c ,因为氯气有毒,且 FeCl 3 易潮解,因此 c→f ,据此解题。
【详解】
(1) 装碱石灰的仪器为干燥管或球形干燥管,碱石灰的作用是除去未反应的氯气,以及防止空气中水蒸气进入收集器;
故答案为:干燥管或球形干燥管。
(2) 浓盐酸易挥发,制取的氯气中会混有氯化氢气体,饱和食盐水的作用是除去多余的氯化氢;
故答案为:除去多氯气中的氯化氢气体。
(3)H 2 O 2 具有强氧化性,可能 KSCN 被 H 2 O 2 氧化了,所以假设 I 为 H 2 O 2 氧化 KSCN ;
实验 ① 中,第一份滴加 FeCl 3 溶液无明显变化;说明没有 KSCN ;第二份滴加试剂 X ;溶液出现红色,说明溶液中存在 Fe 3+ ;第三份滴加稀盐酸和 BaCl 2 溶液,产生白色沉淀,说明反应后溶液中存在硫酸根离子,证明 KSCN 被氧化;所以假设 1 错误;实验 ② 中,另取同浓度的 FeCl 3 溶液滴加 2 滴试剂 X ,溶液变红,再通入 O 2 ;无明显变化,说明 O 2 不会氧化 KSCN ,氧化 KSCN 的为 H 2 O 2 ;假设 II 错误,假设 Ⅲ 正确;
故答案为: H 2 O 2 氧化 KSCN ; I ;证明假设 II 不成立; III 。