人体血液里 的浓度一般采用
来表示。抽取一定体积的血样,加适量的草酸铵
溶液,可析出草酸钙
沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸 (
) ,再用
溶液滴定即可测定血液样品中
的浓度。某研究性学习小组设计如下实验步骤测定血液样品中
的浓度。
Ⅰ . 配制 标准溶液:如图所示是配制
标准溶液的过程示意图。
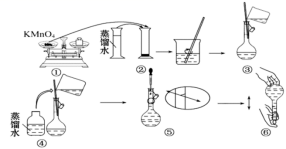
( 1 )请你观察图示判断,其中不正确的操作有 ______ (填序号)。
( 2 )其中步骤⑤中所使用的玻璃仪器有 _____ (填名称)。
( 3 )如果定容时不小心加水超过刻度线,正确的操作是 _______ 。
Ⅱ . 测定血液样品中 的浓度:抽取血样
,经过上述处理后得到草酸,再用
溶液滴定,使草酸转化成
逸出,这时共消耗
溶液。
( 4 )已知草酸跟 反应的离子方程式如下:
,则方程式中的
_____ 。
( 5 )经过计算,血液样品中 的浓度为 ______
。
答案
②⑤ 50mL 容量瓶、胶头滴管 重新配制 2 1.2
【分析】
配制一定物质的量浓度的溶液的实验步骤为计算、称量、溶解、转移、洗涤、定容、摇匀、装瓶贴签,根据正确的实验操作进行判断,根据 CaC 2 O 4 、 H 2 C 2 O 4 、 之间的物质的量关系计算。
【详解】
(1) 由图可知 ②⑤不正确,②不能在量筒中溶解固体,⑤定容时应平视刻度线,至溶液凹液面最低处与刻度线相切,答案:②⑤;
(2) 由图可知 ⑤为定容,由题目要求配制 50mLKMnO 4 标准溶液可知所需玻璃仪器有 50mL 容量瓶、胶头滴管,答案: 50mL 容量瓶、胶头滴管;
(3) 如果定容时不小心加水超过刻度线,导致所配制溶液浓度偏小,正确的操作是重新配制,答案:重新配制;
(4) 根据离子反应中应该遵循电荷守恒可知: 2 (-1)+6
(+1)=2
(+x) ,解得 x=2 ,答案: 2 ;
(5) 血样 20.00 mL 经过上述处理后得到草酸,草酸消耗的高锰酸钾的物质的量为 0.020 mol·L -1 ×0.012 L=2.4×10 -4 mol ,根据反应方程式 及草酸钙的化学式 CaC 2 O 4 ,可知 :n(Ca 2+ )=n(H 2 C 2 O 4 )=n(
)=2.5×2.4×10 -4 mol=6×10 -4 mol , Ca 2+ 的质量为 40 g·mol -1 ×6×10 -4 mol=0.024 g ,钙离子的浓度 =
=
=1.2 mg·cm -3 ,答案: 1.2 。
【点睛】
计算所需溶质多少时应该用所选容量瓶的体积大小来计算。


