下列实验操作中,可用于分离四氯化碳和氯化钠溶液的操作是 ( )
A . 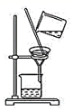 B .
B . 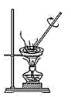 C .
C .  D .
D . 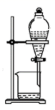
D
【分析】
四氯化碳和氯化钠溶液不互溶,二者会分层,故应该使用分液分离,由此分析。
【详解】
A .该操作为使用过滤的方法分离固体与液体混合物,故 A 不符合题意;
B .该操作为蒸发,蒸发使挥发性溶剂与不挥发性溶质分离的物理操作过程,故 B 不符合题意;
C .该操作为配制一定物质的量浓度的溶液,故 C 不符合题意;
D .分液用来分离两种互不相溶的液体,四氯化碳和氯化钠溶液不互溶,二者会分层,故应该使用分液分离,故 D 符合题意;
答案选 D 。
对于下列化学用语表述正确的是 ( )
A . 的摩尔质量是 40g
B . 摩尔是宏观物质的质量的单位
C . 同温同压下, 1mol 和
的混合气体与 1mol
所占的体积相同
D . 配制 240mL 0.1mol/L 溶液只能用 240mL 的容量瓶进行配制
C
【详解】
A . NaOH 的摩尔质量是 40g/mol , A 错误;
B .摩尔是物质的量的单位,质量的单位是克、千克等, B 错误;
C .根据阿伏伽德罗定律可知,同温同压下, 1mol 任何气体所占的体积都相同, C 正确;
D .配置 240mL 0.1mol/L NaOH 溶液,需要使用 250mL 的容量瓶进行配置, D 错误;
故选 C 。
下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 除去 Na 2 CO 3 粉末中 NaHCO 3 | 溶于水,加入过量 NaOH 溶液 |
| B | 制备少量 Cl 2 | MnO 2 和稀盐酸混合共热 |
| C | 证明还原性: Fe 2+ > Br - | 向 10 mL0.1 mol/LFeBr 2 溶液中滴加 1 mL0.1 mol/L 新制氯水,再滴几滴 KSCN 溶液 |
| D | 配 250 mL0.4 mol/LNaOH 溶液 | 向 250 mL 容量瓶中加入 4 g NaOH 并加水至刻度线 |
A . A B . B C . C D . D
C
【详解】
A . NaHCO 3 与 NaOH 反应生成 Na 2 CO 3 ,但是加入过量 NaOH 溶液,会引入杂质 NaOH , A 错误;
B . 通常用 MnO 2 和浓盐酸混合共热制备少量 Cl 2 , MnO 2 和稀盐酸不反应, B 错误;
C .向 10 mL0.1 mol/LFeBr 2 溶液中滴加 1 mL0.1 mol/L 新制氯水,氯水是不足的,若滴几滴 KSCN 溶液后,溶液呈红色,说明 Fe 2+ 被氧化为 Fe 3+ , Br - 没有被氧化,而一种氧化剂与多种还原剂反应时,先与还原性强的物质反应,则证明还原性: Fe 2+ > Br - , C 正确;
D . 容量瓶必须在规定的温度下使用,通常为室温,不能用于溶解固体或稀释浓溶液,需要先在烧杯中溶解 NaOH 固体,冷却至室温后,再转移至容量瓶中,再洗涤烧杯、玻璃棒,减少溶质损失,再进行定容, D 错误;
故选 C 。
下列实验操作中,主要 不是 从安全因素考虑的是 ( )
A . 点燃氢气前一定要检验氢气的纯度
B . 未使用完的金属钠要放回原试剂瓶中
C . 配制 0.5 的氯化钠溶液时,不能在容量瓶中直接溶解
D . 用氢气还原氧化铜时,要先通一会儿氢气,再加热氧化铜
C
【详解】
A .氢气不纯容易发生爆炸, A 不符合题意;
B . Na 属于遇湿易燃易爆金属,故未用完的 Na 需放回原瓶, B 不符合题意;
C .不在容量瓶中直接溶解固体,是为了防止因固体溶解产生的热效应而引起溶液体积变化,对实验结果产生误差,而不是从安全角度考虑, C 符合题意;
D .通 H 2 可将装置中空气赶尽,防止因混有空气而使 H 2 爆炸, D 不符合题意;
故答案选 C 。
实验室进行自来水的蒸馏实验, 不需要 用到的仪器是 ( )
A . 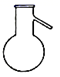 B .
B .  C .
C . ![]() D .
D . ![]()
B
【分析】
蒸馏装置中需要用到酒精灯、蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶等。
【详解】
A .是蒸馏烧瓶,需要用到, A 不合题意;
B .是容量瓶用于配溶液,蒸馏不需要用到, B 符合题意;
C .是冷凝管,需要用到, C 不合题意;
D .是牛角管,需要用到, D 不合题意;
故答案为: B 。
本卷还有95题,登录并加入会员即可免费使用哦~

该作品由: 用户赵潮分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。