某化学小组甲同学学习了酸、碱,盐化学性质后展开了如下探究活动:
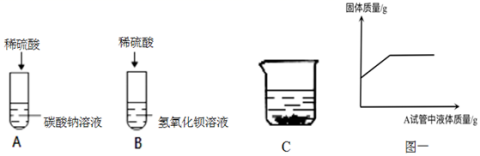
(1)B 试管中发生反应的离子方程式 ___________ 。
(2) 【 实验一 】 A 、 B 试管中物质分别分反应后,先将 B 试管中所有物质倒入空烧杯 C 中,再将 A 试管中所得溶液慢慢滴加到 C 烧杯中,烧杯内固体质量随 A 试管中加入液体质量变化如图一所示;据此判断 B 试管中反应后所得溶液中溶质是 ________ ( 填化学式 ) 。
(3) 【 实验二 】 将 C 烧杯中沉淀过滤,向滤渣中加入过量稀硝酸,观察到 ________ 的实验现象,进而证明滤渣为混合物。
(4) 【 猜想与假设 】 C 烧杯滤液中含有哪些离子?
猜想一: Na + 、 Ba 2+ 、 OH -
猜想二: Na + 、 H + 、
猜想三: Na + 、 OH - 、
猜想四: Na + 、 OH - 、
猜想五: ① _____________ ( 写出一种即可 ) ;
②小组同学一致认为猜想 ________ 不正确,理由是 ____________ 。
(5) 【 实验探究 】 为确定最终滤液中溶质成分,小组同学向滤液中加入稀硫酸,观察到 ________ 的实验现象,最终证明了溶液的溶质成分。
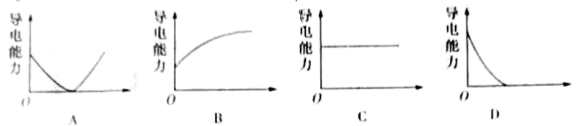
(6) 向 溶液中滴加稀 H 2 SO 4 反应至过量,导电能力随时间变化的曲线图为 ________ ( 字母代号 ) 。
答案
+2H + +Ba 2+ +2OH - =BaSO 4 ↓+2H 2 O Ba(OH) 2 沉淀部分溶解,有气泡产生 Na + 、 OH - 或 (Na + 、 OH - 、
、
) 二 H + 与
不能共存且 BaCO 3 能溶于强酸,滤液中不含有 H + 白色沉淀 A
【详解】
(1)B 试管中氢氧化钡与硫酸反应生成硫酸钡沉淀和水,发生反应的离子方程式为 +2H + +Ba 2+ +2OH - =BaSO 4 ↓+2H 2 O ,故答案为:
+2H + +Ba 2+ +2OH - =BaSO 4 ↓+2H 2 O ;
(2) 先将 B 试管中所有物质倒入空烧杯 C 中,再将 A 试管中所得溶液慢慢滴加到 C 烧杯中,烧杯内固体质量随 A 试管中加入液体质量增大而增加,说明有沉淀生成,沉淀可能是碳酸钡沉淀、硫酸钡沉淀、碳酸钡沉淀和硫酸钡沉淀混合;由此可知, B 试管中稀硫酸少量被反应完了,氢氧化钡溶液过量有剩余,反应后所得溶液中的溶质是 Ba(OH) 2 ,故答案为: Ba(OH) 2 ;
(3) 将 C 烧杯中沉淀过滤,向滤渣中加入过量稀硝酸,碳酸钡与硝酸发生反应生成硝酸钡、二氧化碳、水,而硫酸钡沉淀不溶于稀硝酸,观察到沉淀部分溶解,有气泡产生,进而证明滤渣为混合物;故答案为:沉淀部分溶解,有气泡产生;
(4) ① A 、 B 试管内加入碳酸钠、硫酸、氢氧化钡,所以 C 烧杯滤液中含的离子可能是 Na + 、 OH - 或 (Na + 、 OH - 、 、
) ;故答案为: Na + 、 OH - 或 (Na + 、 OH - 、
、
) ;
② H + 、 反应生成二氧化碳气体,所以 H + 、
不能共存, BaCO 3 能溶于强酸,滤液中不含有 H + ,故猜想二不正确;故答案为:二; H + 与
不能共存且 BaCO 3 能溶于强酸,滤液中不含有 H + ;
(5) 硫酸根离子和钡离子反应生成硫酸钡沉淀,向滤液中加入稀硫酸,观察到有白色沉淀生成,因此可以推测猜想一正确,最终证明了溶液的溶质成分;故答案为:白色沉淀;
(6) 氢氧化钡与硫酸反应生成硫酸钡沉淀和水,向 Ba(OH) 2 溶液中滴加稀 H 2 SO 4 反应至过量,恰好完全反应时,离子浓度接近为 0 , H 2 SO 4 过量后离子浓度增大,离子浓度先减后增,导电能力先减后增,故选 A 。

 NH3↑+H2O;NH3+H2O
NH3↑+H2O;NH3+H2O NH3·H2O
NH3·H2O NH4++OH-
NH4++OH-  CuO+H2O
CuO+H2O