亚硝酰氯 (NOCl) 常用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成亚硝酰氯。
已知: ① NOCl 是黄色气体,熔点: -64.5 ℃,沸点: -5.5 ℃; NOCl 遇水易反应生成一种无氧酸和两种氮的常见氧化物; NOCl 对眼睛、皮肤和粘膜有强烈刺激性,具有类似氯气和氮氧化物的毒作用。
② Ag 2 CrO 4 是砖红色沉淀。
实验 1 :制备原料气 NO 和 Cl 2
利用如图所示装置制备纯净的 NO 和 Cl 2 。
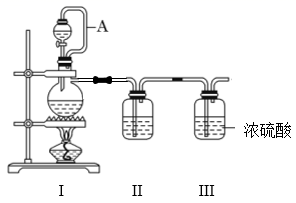
(1) 制备纯净的 Cl 2 ,烧瓶中反应的化学方程式为 __ 。
(2) 制备纯净的 NO ,烧瓶中盛有 Cu ,装置 Ⅱ中盛有 __ ( 填试剂名称 ) 。
实验 2 :制备 NOCl 。
利用实验 1 中制得的 NO 和 Cl 2 制备 NOCl ,装置如图所示。

(3) 仪器接口的连接顺序为 a→ __ ( 按气流从左到右顺序填写 ) 。
(4) 装置 Ⅶ的仪器名称为 ___ ,装置 Ⅳ、Ⅴ除进一步干燥 NO 和 Cl 2 外,另一作用是 __ 。
(5) 装置 Ⅷ用于吸收尾气, NOCl 发生反应的化学方程式为 __ 。
实验 3 :测定 NOCl 的纯度
将所得亚硝酰氯 (NOCl) 产品 13.1g 溶于水,配成 250ml 该溶液,取出 25.00mL 该溶液,以 K 2 CrO 4 溶液为指示剂,用 1.0mol/LAgNO 3 标准溶液滴定至终点,再重复上述实验操作 2 次,测得三次实验消耗 AgNO 3 标准溶液的平均体积为 19.22mL 。
(6) 达到滴定终点的现象是 ___ 。
(7) 产品中亚硝酰氯 (NOCl) 的质量分数为 __ ( 保留两位小数 ) 。
答案
2KMnO 4 +16HCl( 浓 )=2KCl+2MnCl 2 +5Cl 2 ↑+8H 2 O 或 KClO 3 +6HCl( 浓 )=KCl+3Cl 2 ↑+3H 2 O 水 e→f( 或 f→e)→c→b→d 球形干燥管 通过观察气泡,调节 NO 和 Cl 2 的流速 NOCl+2NaOH=NaCl+NaNO 2 +H 2 O 出现砖红色沉淀 96.10%
【分析】
实验室制备 NO ,可用稀硝酸与铜在常温下反应;无加热装置制氯气,可用浓盐酸和强氧化剂如高锰酸钾、氯酸钾制备氯气;二者混合制取亚硝酰氯,亚硝酰氯熔沸点较低,在制备时要注意低温环境;未测得产品的纯度可采用氧化还原滴定进行滴定分析,据此解答。
【详解】
(1) 常用浓盐酸和强氧化剂制备氯气,该装置无加热装置,故烧瓶中制备纯净的 Cl 2 的化学方程式为: 2KMnO 4 +16HCl (浓) =2KCl+2MnCl 2 +5Cl 2 ↑+8H 2 O 或 KClO 3 +6HCl (浓) =KCl+3Cl 2 ↑+3H 2 O ;
(2) 制备纯净的 NO ,烧瓶中盛有 Cu ,装置 Ⅱ 中盛水;
(3) 制备 NOCl , NOCl 的熔沸点较低,要保持低温环境,且最后进行尾气处理,干燥管的气流方向是大进小出,故仪器接口的连接顺序为 a→e→f( 或 f→e)→c→b→d ;
(4) Ⅶ的仪器名称为球形干燥管;装置 Ⅳ 、 Ⅴ 除进一步干燥 NO 和 Cl 2 外,另一作用是:通过观察气泡,调节 NO 和 Cl 2 的流速;
(5) NOCl 遇水易反应生成一种无氧酸和两种氮的常见氧化物,故 NOCl 与氢氧化钠反应: NOCl+2NaOH=NaCl+NaNO 2 +H 2 O ;
(6) 滴定终点,可生成 Ag 2 CrO 4 , 有砖红色沉淀生成 , 终点现象为当滴入最后一滴 AgNO 3 标准溶液,溶液中有砖红色沉淀产生,且 30s 不消失;
(7) 取产品 13.1g 溶于水,配成 250mL 该溶液,取出 25.00mL ,则混合溶液中满足: , 250mL 原溶液的 NOCl 物质的量为:
,所以产品中亚硝酰氯( NOCl )的质量分数为:
。



 N2+3Cu+3H2O
N2+3Cu+3H2O