兴趣小组将氯气通入水中制得氯水并对氯水的成分和性质进行研究,实验如下:
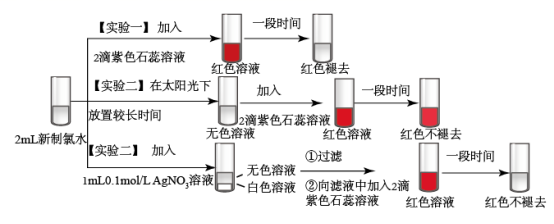
(1) 实验一的现象表明,氯水具有酸性和 _______ 性。
(2) 用化学方程式说明实验二中 “ 红色不褪去 ” 的原因 _______ 。
(3) 在讨论实验三中 “ 红色不褪去 ” 的原因时,润祺同学认为是氯水和硝酸银溶液反应生成 AgCl 和 _______ 白色沉淀;戈同学认为是银离子作催化剂使 HClO 分解。
答案
漂白或氧化 Cl 2 +2AgNO 3 +H 2 O= AgCl ↓ +AgClO ↓ +2HNO 3
【详解】
(1) 实验一:酸能使紫色石蕊试液变红色,氯水能使红色的溶液褪色,氯水中加入紫色石蕊试液后变红色说明溶液呈酸性,后来溶液褪色,说明具有漂白或氧化性,故答案为:漂白或氧化;
(2) 红色不褪去,说明溶液光照后不存在 HClO ,因为 HClO 不稳定,光照易分解生成 HCl 和氧气,反应方程式为 ;
(3) 氯气和水反应有 HClO 生成,则沉淀中应该含有 AgClO ,反应方程式为 Cl 2 +2AgNO 3 +H 2 O= AgCl ↓ +AgClO ↓ +2HNO 3 。

 NH3↑+H2O;NH3+H2O
NH3↑+H2O;NH3+H2O NH3·H2O
NH3·H2O NH4++OH-
NH4++OH-  CuO+H2O
CuO+H2O