在 25 ℃、 101kPa 的条件下,断裂 1molH—H 键吸收 436kJ 能量,断裂 1molCl—Cl 键吸收 243kJ 能量,形成 1molH-Cl 键放出 431 kJ 能量。 H 2 +Cl 2 =2HCl 的化学反应可用如图表示:
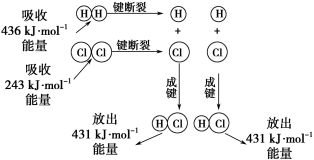
请回答下列有关问题:
(1) 反应物断键吸收的总能量为 ___________________ 。
(2) 生成物成键放出的总能量为 ______________ 。
(3) 判断 H 2 +Cl 2 =2HCl 反应 _____________ ( 填 “ 吸收 ” 或 “ 放出 ”) 能量。
(4) 反应物的总能量 ________ ( 填 “ > ” 、 “=” 或 “ < ”) 生成物的总能量。
答案
679kJ 862kJ 放出 >
【分析】
(1) 反应物断键吸收的总能量为氢气和氯气的键能和;
(2) 生成物成键放出的总能量为 2molHCl 的总键能;
(3) 根据生成物的键能的和与反应物的键能的和的大小关系判断、分析比较。
【详解】
(1) 反应物断键吸收的总能量为氢气和氯气的键能和,则反应物断键吸收的总能量为 436kJ+243kJ=679kJ ;
(2) 生成物成键放出的总能量为形成 2molHCl 的总键能,则生成物成键放出的总能量为 431kJ×2=862kJ ;
(3) 断键吸收的总能量是 679kJ ,形成 2molHCl 释放的总能量是 862kJ ,吸收的能量少,放出的能量多,因此该反应是放出热量的反应;
(4) 反应放出热量,说明反应物的总能量大于生成物的总能量。
【点睛】
本题主要考查了化学反应与能量的变化的知识,化学反应过程中既有物质变化,也有能量变化。断裂反应物化学键吸收能量,形成生成物化学键释放能量,反应是放热反应还是吸热反应取决于断键吸收的能量与成键释放的能量差。任何反应发生都有断裂化学键吸收能量的过程,与反应放热还是吸热无关。
