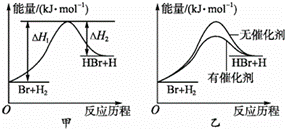
已知:氧化锂( Li 2 O )晶体形成过程中的能量变化如图所示

下列说法正确的是
A . △ H 1 <0 , △ H 2 >0 B . - △ H 5 + △ H 1 + △ H 2 + △ H 3 + △ H 4 + △ H 6 =0
C . △ H 3 <0 , △ H 4 <0 D . △ H 1 + △ H 2 + △ H 3 + △ H 4 = △ H 5 + △ H 6
答案
B
【详解】
A . Li 晶体转化为 Li(g) 是吸热过程, Li(g)→Li + (g) 是失电子过程吸热,即 △ H 1 >0 、 △ H 2 >0 ,故 A 错误;
B .由盖斯定律可知, △ H 1 + △ H 1 + △ H 3 + △ H 4 + △ H 6 = △ H 5 ,即 - △ H 5 + △ H 1 + △ H 2 + △ H 3 + △ H 4 + △ H 6 =0 ,故 B 正确;
C . O 2 (g) 到 O(g) 是键断裂过程吸热, O(g)→O 2- (g) 是得电子过程放热,即 △ H 3 >0 、 △ H 4 <0 ,故 C 错误;
D .由盖斯定律可知, △ H 1 + △ H 2 + △ H 3 + △ H 4 + △ H 6 = △ H 5 ,故 D 错误;
故答案为 B 。