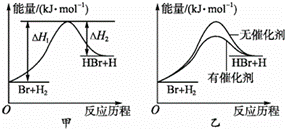
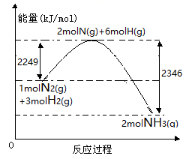
已知拆开 1molH 2 (g) 中的 H-H 键需要消耗 436kJ 能量,如图反应 3H 2 (g)+N 2 (g) ![]() 2NH 3 (g) 的能量变化示意图.下列说法不正确的是
2NH 3 (g) 的能量变化示意图.下列说法不正确的是
A . 断开 1 mol N 2 (g) 中的 N ![]() N 键要吸收 941 kJ 能量
N 键要吸收 941 kJ 能量
B . 生成 2mol NH 3 (g) 中的 N - H 键吸收 2346 kJ 能量
C . 3H 2 (g) + N 2 (g) ![]() 2NH 3 (g) △ H =- 97
2NH 3 (g) △ H =- 97 ![]()
D . NH 3 (g) ![]() 3/2H 2 (g) +1/2 N 2 (g) △ H = 48.5
3/2H 2 (g) +1/2 N 2 (g) △ H = 48.5 ![]()
答案
B
【解析】
A .拆开 1molH 2 (g) 中的 H ﹣ H 键需要消耗 436kJ 能量,图中断裂化学键吸收能量为 2249kJ ,则断开 1 mol N 2 (g) 中的 N≡N 键要吸收能量为 2249kJ ﹣ 436kJ×3 = 941 kJ ,故 A 正确;
B .图中生成 2mol NH 3 (g) 时形成化学键释放的能量为 2346kJ ,而断裂化学键吸收能量,故 B 错误;
C .由图可知 △ H = (2249 ﹣ 2346)kJ/mol =﹣ 97 kJ•mol ﹣ 1 ,即热化学方程式为 3H 2 (g)+N 2 (g) ⇌ 2NH 3 (g) △ H =﹣ 97 kJ•mol ﹣ 1 ,故 C 正确
D .互为逆反应时焓变的数值相同、符号相反,且物质的量与热量成正比,由 3H 2 (g)+N 2 (g) ⇌ 2NH 3 (g) △ H =﹣ 97 kJ•mol ﹣ 1 可知 NH 3 (g) ⇌ ![]() H 2 (g)+
H 2 (g)+ ![]() N 2 (g) △ H = 48.5kJ•mol ﹣ 1 ,故 D 正确;
N 2 (g) △ H = 48.5kJ•mol ﹣ 1 ,故 D 正确;
故答案为 B 。