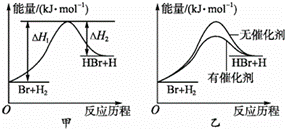
已知断裂 1mol H 2 (g) 中的 H-H 键需要吸收 436.4kJ 的能量,断裂 1mol O 2 (g) 中的共价键需要吸收 498kJ 的能量,生成 H 2 O(g) 中的 1mol H-O 键能放出 462.8kJ 的能量。下列说法正确的是
A . 断裂 1mol H 2 O 中的化学键需要吸收 925.6kJ 的能量
B . 2H 2 (g)+O 2 (g)=2H 2 O(g) ΔH= -480.4kJ/mol
C . 2H 2 O(l)=2H 2 (g)+O 2 (g) ΔH= +480.4kJ/mol
D . H 2 (g)+ O 2 (g)=H 2 O(l) ΔH= -240.2kJ/mol
答案
B
【解析】
A .生成 H 2 O(g) 中的 1mol H-O 键能放出 462.8kJ 的能量,则断裂 1mol H 2 O(g) 中的化学键需要吸收热量 462.8kJ×2=925.6kJ ,但题干中并未说明水的状态, A 错误;
B. 反应热等于断键吸收的能量和形成化学键所放出的能量的差值,则 2H 2 (g)+O 2 (g) = 2H 2 O(g) △ H=436.4kJ/mol×2+498kJ/mol-2×2×462.8kJ/mol= -480.4kJ/mol , B 正确;
C. 已知气态水转化为液态水放热,则 2H 2 (g)+O 2 (g)=2H 2 O(l) △ H < -480.4kJ/mol ,由此可知 2H 2 O(l)=2H 2 (g)+O 2 (g) △ H > +480.4kJ/mol , C 错误;
D.2H 2 O(l)=2H 2 (g)+O 2 (g) △ H > +480.4kJ/mol ,则 H 2 (g)+ O 2 (g)=H 2 O(l) △ H < -240.2kJ/mol , D 错误;
答案选 B 。
【点睛】
本题考查反应热与焓变,为高频考点,把握反应中能量变化、焓变的计算为解答的关键。注意气态水转化为液态水为放热;焓变等于断键吸收的能量减去成键释放的能量,且物质的量与热量成正比,互为逆反应时焓变的数值相同、符号相反,答题时需要灵活应用。