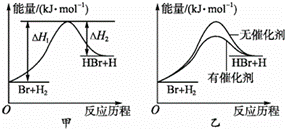
1mol白磷(P 4 , s)和4mol红磷(P,s)与氧气反应过程中的能量变化如图(E表示能量)。下列说法正确的是( )
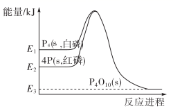
A . P 4 (s,白磷)=4P(s,红磷) ΔH>0
B . 以上变化中,白磷和红磷所需活化能相等
C . 白磷比红磷稳定
D . 红磷燃烧的热化学方程式是 4P(s,红磷)+5O 2 (g)=P 4 O 10 (s) ΔH=-(E 2 - E 3 )kJ/mol
答案
D
【详解】
A .依据图象分析,白磷能量高于红磷,依据能量守恒,白磷转变为红磷是放热反应,则 ΔH < 0 ,故 A 错误; B .依据图象分析,白磷能量高于红磷,则白磷和红磷所需活化能不相等,故 B 错误; C .依据图象分析,白磷能量高于红磷,能量低的稳定,则红磷稳定,故 C 错误; D .依据图象分析,红磷燃烧是放热反应,则反应的热化学方程式: 4P(s ,红磷 ) + 5O 2 (g) = P 4 O 10 (s) ΔH= - (E 2 - E 3 )kJ/mol ,故 D 正确;故答案为 D 。