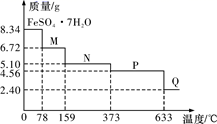
草酸晶体的组成可表示为H2C2O4·xH2O,某研究性学习小组用下图装置进行“草酸晶体受热分解的部分产物的验证”的实验。请回答下列问题。
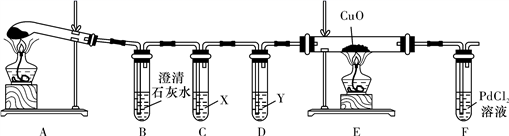
(资料查阅)
①草酸晶体在101 ℃时开始熔化,150 ℃时开始升华,175 ℃时开始分解;
②草酸钙和草酸氢钙均为白色不溶物。
(1)按照如图所示的装置,通过实验检验草酸晶体的部分分解产物,装置B中可观察到有气泡冒出且澄清石灰水变浑浊,由此甲同学判断草酸晶体分解的产物中有CO2。但立即遭到乙同学反对,其反对的理由可能是______________________________________。
(2)丙同学认为草酸晶体分解的产物中含有CO,为进行验证,X应选用________(填化学式)浓溶液,装置D的作用是____________________。
(3)实验过程中涉及如下操作:①点燃装置A处的酒精灯;②熄灭装置A处的酒精灯;③点燃装置E处的酒精灯;④熄灭装置E处的酒精灯。这4步操作由先到后的顺序为____________(填序号)。点燃E处酒精灯前必须要进行的操作是______________。
(4)实验过程中发现装置E中黑色粉末变红色,装置F中有黑色固体生成,经检测装置F中的固体为金属单质,则装置F中发生反应的化学方程式为________________________________________________________________________。
(5)丁同学用滴定法测定草酸晶体中结晶水的含量,进行了下列操作:
步骤一:用分析天平称取3.15 g纯净的该草酸晶体,配制成250 mL溶液。
步骤二:用移液管移取25.00 mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化。
步骤三:取0.100 mol·L-1标准酸性KMnO4溶液,进行滴定,三次结果如下表所示:
| 第一次 | 第二次 | 第三次 | |
| 待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
| 标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
已知滴定反应的离子方程式为:MnO![]() +H2C2O4+H+—→Mn2++CO2↑+H2O(未配平)。
+H2C2O4+H+—→Mn2++CO2↑+H2O(未配平)。
①配制草酸溶液的操作步骤依次是:将晶体置于烧杯中,加水溶解,将溶液转移入________,洗涤,定容,摇匀。
②通过计算确定x=________。
答案
挥发出的草酸与澄清石灰水反应也产生相同的现象(或因为草酸钙、草酸氢钙都为白色沉淀) NaOH 干燥CO(或除去CO中的水蒸气) ①③④② 检验CO的纯度 PdCl2+H2O+CO===Pd↓+CO2+2HCl 250 mL容量瓶 2
【解析】
(1)草酸晶体在101℃时开始熔化,150℃时开始升华,因此加热分解时,挥发出的草酸与澄清石灰水反应也产生白色沉淀;正确答案:挥发出的草酸与澄清石灰水反应也产生相同的现象(或:因为草酸钙、草酸氢钙都为白色沉淀)。
(2)草酸受热分解,可能产生CO和CO2,因此,在验证CO气体之前,先除去CO2,X应选用NaOH溶液, 干燥的CO能够还原氧化铜,因此,必须用浓硫酸干燥CO气体,正确答案:NaOH;干燥CO(或:除去CO中的水蒸气)。
(3)先点燃A处的酒精灯,产生气体,排净装置内空气,然后加热E装置反应发生,反应结束后,先熄灭E处酒精灯,冷却至室温后,在熄灭A处的酒精灯,以防产生倒吸;所以这4步操作由先到后的顺序为①③④②;点燃E处酒精灯前必须要进行的操作是检验CO的纯度;正确答案:①③④②;检验CO的纯度,(体现“验纯”)。
(4)PdCl2与多余的CO反应生成金属Pd,CO被氧化为CO2;化学方程式为PdCl2+H2O+CO=== Pd↓+CO2+2HCl;正确答案:PdCl2+H2O+CO=== Pd↓+CO2+2HCl;
(5)消耗KMnO4溶液的体积为9.99+10.01+10.00=10.00mL,消耗KMnO4的量为0.10×10×10-3=10-3 mol,25 mL草酸溶液消耗KMnO410-3 mol,250 mL草酸溶液消耗KMnO410-2 mol;反应如下:2MnO4—+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,根据反应关系2MnO4—--5H2C2O4,消耗H2C2O4的量为2.5×10-2 mol,3.15g纯净H2C2O4·xH2O的量为2.5×10-2 mol,3.15/(90+18x)= 2.5×10-2, x=2;正确答案:2。



 N2+3Cu+3H2O
N2+3Cu+3H2O