分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是
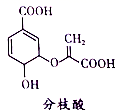
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
B
【详解】
A项,该化合物分子中含有羧基、醇羟基、醚键和碳碳双键4种官能团,故A项错误;
B项,该物质中含有羧基和羟基,既可以与乙醇发生酯化反应,也可以与乙酸发生酯化反应,反应类型相同,故B项正确;
C项,分枝酸中只有羧基能与NaOH溶液发生中和反应,一个分子中含两个羧基,故1mol分枝酸最多能与2mol NaOH发生中和反应,故C项错误;
D项,该物质使溴的四氯化碳溶液褪色的原理是溴与碳碳双键发生加成反应,而是使酸性高锰酸钾溶液褪色是发生氧化反应,原理不同,故D项错误。
综上所述,本题正确答案为B。
【点睛】
本题考查了有机化合物的结构与性质,包含了通过分析有机化合物的结构简式,判断有机化合物的官能团、反应类型的判断、有机物的性质,掌握官能团的性质是解题的关键。
苹果酸的结构简式为![]() ,下列说法正确的是
,下列说法正确的是
A.苹果酸中能发生酯化反应的官能团有2种
B.1mol苹果酸可与3mol NaOH发生中和反应
C.1mol苹果酸与足量金属Na反应生成生成1mol H2
D.HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
A
【详解】
A.该分子中含有羧基和醇羟基,所以能发生酯化反应的官能团有羧基和醇羟基,所以苹果酸中能发生酯化反应的官能团有2种,A正确;
B.1mol苹果酸中含有2mol羧基,所以1mol苹果酸可与2molNaOH发生中和反应,B错误;
C.能和Na反应是有羧基和醇羟基,1mol苹果酸与足量金属Na反应生成1.5molH2,C错误;
D.HOOC-CH2-CH(OH)-COOH与苹果酸是同一种物质,D错误。
答案选A。
某有机物的结构简式如图,下列关于该有机物的说法正确的是( )

A.分子式为C7H6O5
B.1 mol该物质能与4 mol Na发生反应
C.分子中含有两种官能团
D.在水溶液中羧基和羟基均能电离出H+
B
【详解】
A.分子式为C7H10O5,故A错误;B.1 mol该物质含有3个羟基和1个羧基,能与4 mol Na发生反应,故B正确;C. 分子中含有C=C、-COOH和-OH三种官能团,故C错误;D. 在水溶液中羧基能电离出H+,羟基不能电离出H+,故D错误;答案:B。
【点睛】
根据官能团判断相应的性质。含有-COOH和-OH能和金属钠反应,根据结构简式判断分子式。
丙烯酸可与水反应生成乳酸,化学方程式如下。下列说法正确的是

A.该反应为加成反应,没有副产物生成
B.可用Br2的CCl4溶液鉴别丙烯酸和乳酸
C.丙烯酸与乳酸都属于有机酸,两者不发生反应
D.l mol乳酸分别与足量Na、NaOH、NaHCO3反应,消耗三者物质的量之比为2:2:1
B
【解析】
A.该反应为加成反应,但加成产物有两种,其中一种HOCH2CH2COOH为副产物生成,故A错误;B.丙烯酸结构中有碳碳双键,而乳酸没有碳碳双键,可用可用Br2/CCl4溶液鉴别这两种有机物,故B正确;C.丙烯酸与乳酸都属于有机酸,羧基之间可以脱水生成酸酐,故C错误;D.羧基能与Na、NaOH、NaHCO3反应,而羟基只与Na反应,则1mol乳酸分别与足量Na、NaOH、NaHCO3反应,消耗三者物质的量之比为2:1:1,故D错误;答案为B。
蓓萨罗丁是一种治疗顽固性皮肤T细胞淋巴瘤的药物,其结构如图所示。下列有关说法正确的是
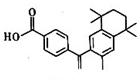
A.分子中所有碳原子在同一平面内
B.既能发生加成反应,又能发生消去反应
C.能使溴水、酸性高锰酸钾溶液褪色,且原理相同
D.1mol蓓萨罗丁分别与足量的Na、 NaHCO3反应,产生气体的物质的量之比为l︰2
D
【解析】
A.右边苯环上方的第一个碳与周围四个碳原子均为单键结构,为四面体构型,不可能所有碳原子在同一平面内,故A错误;
B.分子中含有碳碳双键能发生加成反应,但没有可发生消去反应的官能团,故B错误;
C.碳碳双键使溴水褪色发生的是加成反应,而其使酸性高锰酸钾褪色发生的是氧化反应,故C错误;
D.1mol蓓萨罗丁与足量的Na反应生成0.5molH2,而其与足量NaHCO3反应生成1mol的CO2,产生气体的物质的量之比为l︰2,故D正确。
本题选D。
本卷还有95题,登录并加入会员即可免费使用哦~

该作品由: 用户姚怡含分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。