下列叙述正确的是
A.HClO 的结构式为H-Cl-O
B.核内有33个中子的Fe表示为![]() Fe
Fe
C.NH2OH的电子式为 
D.CH3CHO 的球棍模型为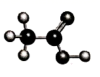
答案
C
【详解】
A. HClO 的结构式为H-O-Cl,故A错误;
B. 核内有33个中子的Fe原子质量数为:33+26=59,表示为![]() Fe,故B错误;
Fe,故B错误;
C. NH2OH的电子式为 ,故C正确;
,故C正确;
D. CH3CHO 的球棍模型为 ,故D错误;
,故D错误;
正确答案是C。
下列叙述正确的是
A.HClO 的结构式为H-Cl-O
B.核内有33个中子的Fe表示为![]() Fe
Fe
C.NH2OH的电子式为 
D.CH3CHO 的球棍模型为
C
【详解】
A. HClO 的结构式为H-O-Cl,故A错误;
B. 核内有33个中子的Fe原子质量数为:33+26=59,表示为![]() Fe,故B错误;
Fe,故B错误;
C. NH2OH的电子式为 ,故C正确;
,故C正确;
D. CH3CHO 的球棍模型为 ,故D错误;
,故D错误;
正确答案是C。
原子是否满足最外层8电子结构的判断方法:
1.离子化合物
(1)阳离子:看“主族元素原子的次外层电子数+ 原子的最外层电子数一化合价数”是否等于8,若为8,则该原子满足最外层8电子结构,否则不满足。
(2)阴离子:看“其原子的最外层电子数+化合价的绝对值”是否等于8,若为8,则该原子满足最外层8 电子结构,否则不满足。
2.共价化合物计算“各原子的最外层电子数+化合价的绝对值” 是否等于8,若为8,则该原子满足最外层8电子结构,否则不满足。另外,还有一些不满足8电子结构的特殊粒子,请大家记住:
(1)主族元素形成的化合物中:
a.H、Li、Be、B元素原子不满足最外层8电子结构.
b.非最高价离子(如 Pb2+、Bi3+等)也不满足最外层8电子结构。
(2)过渡金属元素形成的离子最外层电子数一般大于8.
登录并加入会员可无限制查看知识点解析