根据下列图示所得出的结论不正确的是
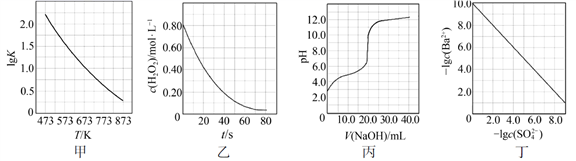
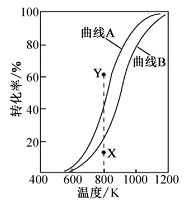
A.图甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
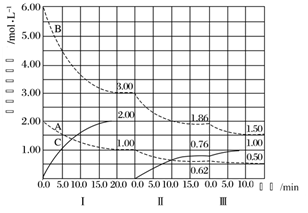
B.图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
C.图丙是室温下用0.1000 mol·L−1NaOH溶液滴定20.00 mL 0.1000 mol·L−1某一元酸HX的滴定曲线,说明HX是一元强酸
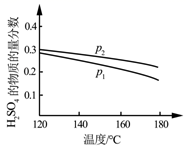
D.图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42−)的关系曲线,说明溶液中c(SO42− )越大c(Ba2+ )越小
答案
C
【解析】
A. 升高温度,lgK减小,平衡向逆反应方向移动,逆反应为吸热反应,正反应为放热反应,该反应的ΔH![]() 0;
0;
B. 根据图像,随着时间的推移,c(H2O2)变化趋于平缓,随着反应的进行H2O2分解速率逐渐减小;
C. 根据图像,没有滴入NaOH溶液时,0.1000mol/LHX溶液的pH![]() 1,HX为一元弱酸;
1,HX为一元弱酸;
D. 根据图像可见横坐标越小,纵坐标越大,-lgc(SO42-)越小,-lgc(Ba2+)越大,说明c(SO42-)越大c(Ba2+)越小。
【详解】
A. 升高温度,lgK减小,平衡向逆反应方向移动,逆反应为吸热反应,正反应为放热反应,该反应的ΔH![]() 0,A项正确;
0,A项正确;
B. 根据图像,随着时间的推移,c(H2O2)变化趋于平缓,随着反应的进行H2O2分解速率逐渐减小,B项正确;
C. 根据图像,没有滴入NaOH溶液时,0.1000mol/LHX溶液的pH![]() 1,HX为一元弱酸,C项错误;
1,HX为一元弱酸,C项错误;
D. 根据图像可见横坐标越小,纵坐标越大,-lgc(SO42-)越小,-lgc(Ba2+)越大,说明c(SO42-)越大c(Ba2+)越小,D项正确;
答案选C。
【点睛】
本题考查图像的分析,侧重考查温度对化学平衡常数的影响、化学反应速率、酸碱中和滴定pH曲线的分析、沉淀溶解平衡曲线的分析,掌握有关的原理,明确图像中纵、横坐标的含义和曲线的变化趋势是解题的关键。

 pC(g)+qD(g)
pC(g)+qD(g)  。
。 时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。
时,平衡便会发生移动而使各组分的浓度、百分含量发生变化,直至建立新的平衡。 指的是同一物质的正反应速率与逆反应速率相等。
指的是同一物质的正反应速率与逆反应速率相等。  qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。
qD(g),根据对化学平衡概念的理解,判断下列各情况是否达到平衡。