设NA表示阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,6.4 g O2和O3的混合气体中含有的原子数为0.4NA
B.100 mL l mol·L-1的碳酸钠溶液中含有的CO32-数为0.1NA
C.标准状况下,2.24 L苯中含有的碳原子数为0.6NA
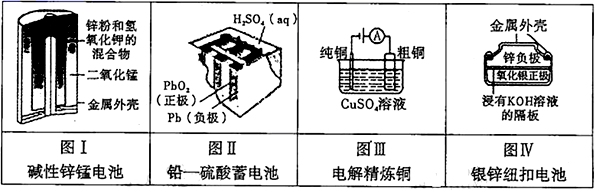
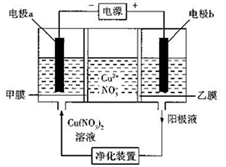
D.用含有少量锌、铁、银等杂质的粗铜作阳极电解精炼铜,当阴极析出64 g金属时,阳极失去的电子数小于2NA
答案
A
【解析】
A.氧气和臭氧均由氧原子构成,故6.4g混合物中含有的氧原子的物质的量n=![]() =0.4mol,个数为0.4NA个,故A正确;B.CO32-在水溶液中要水解,则100 mL l mol·L-1的碳酸钠溶液中含有的CO32-数小于0.1NA,故B错误;C.标准状况下,苯不为液体,不能根据气体摩尔体积计算其物质的量,故C错误;D.依据电极反应和电子守恒分析,当阴极析出64 g金属时,阳极失去的电子数等于2NA,故D错误;故答案为A。
=0.4mol,个数为0.4NA个,故A正确;B.CO32-在水溶液中要水解,则100 mL l mol·L-1的碳酸钠溶液中含有的CO32-数小于0.1NA,故B错误;C.标准状况下,苯不为液体,不能根据气体摩尔体积计算其物质的量,故C错误;D.依据电极反应和电子守恒分析,当阴极析出64 g金属时,阳极失去的电子数等于2NA,故D错误;故答案为A。
【点睛】
阿伏伽德罗常数的常见问题和注意事项:①物质的状态是否为气体;②对于气体注意条件是否为标况;③注意同位素原子的差异;④注意可逆反应或易水解盐中离子数目的判断;⑤注意物质的结构:如Na2O2是由Na+和O22-构成,而不是有Na+和O2-构成;SiO2、SiC都是原子晶体,其结构中只有原子没有分子,SiO2是正四面体结构,1molSiO2中含有的共价键为4NA,1molP4含有的共价键为6NA等.