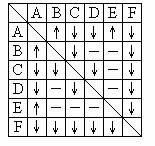
废钯催化剂中含钯 5-6%,碳 93-94%,铁 1-2%,铜 0.1-0.2%以及锌等杂质。在实验室中探究采用废钯催化剂制备无水氯化钯,具体流程如下:

已知:Pd2+、Cu2+、Zn2+等离子均可与氨水生成[M(NH3)n]x+离子,其中[Pd(NH3)2]2+在盐酸中能以[Pd(NH3)2]Cl2 黄色晶体的形式析出。
(1)灼烧钯碳时使用的主要仪器有:酒精灯、玻璃棒、_____(支持仪器省略)。王水溶解过程中会生成 NOCl,NOCl 的结构式为________。
(2)是否进行虚线方框内的操作,对提高钯的回收率至关重要,其主要原因是_____。
(3)最后焙烧之前若不烘干,所得产品中会混有_____杂质。
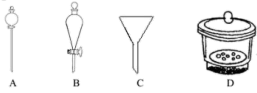
(4)可用“化学放大”法测定样品中的微量 Fe3+:在酸性介质中加入过量的 KI 后用CCl4萃取,分去水相后,用肼(N2H4)的水溶液进行还原并反萃取,还原过程中有无污染的气体生成。再用过量的 Br- 将反萃取出的 I- 氧化成 IO3- ,煮沸除 Br2后,加入过量的 KI,酸化后用Na2S2O3 标准液进行滴定。经上述步骤后,样品含量的测定值放大了_____倍,写出还原过程中发生反应的离子方程式___________,假定萃取达到平衡时,样品在水和萃取剂中的总浓度比为 1∶80,50mL 的水溶液样品,用 10mL 萃取剂萃取,萃取后溶液中残留的样品浓度为原溶液的_______________倍(用分数表示)。完成萃取和反萃取操作,必须选用的仪器有____________(填标号)。
答案
(1). 坩埚 (2). O=N-Cl (3). Fe(OH)3 为胶状沉淀,对[Pd(NH3)2]2+具有很强的吸附作用,若不进行此操作, [Pd(NH3)2]2+的吸附损失大 (4). PdO (5). 6 (6). N2H4+2I2=4I-+N2↑+4H+ (7). 1/17 (8). B
【解析】
废钯催化剂经烘干后,在700℃的高温下焙烧,C、Fe、Pd、有机物被氧气氧化生成氧化物,向氧化物中加入王水,滤渣中含有Pd、SiO2,二氧化硅不溶于王水,但Pd能溶于王水生成溶液,同时生成气体,加入浓氨水调节溶液pH,钯转变为可溶性[Pd(NH3)2]2+,使铁全部沉淀,溶液中加入盐酸酸析得到沉淀,经过脱氨等一系列操作得当氯化钯。
【详解】(1)灼烧固体要在坩埚中进行,灼烧钯碳时使用的主要仪器有:酒精灯、玻璃棒、坩埚。由于NOCl中所有原子都达到了8电子稳定结构,即N形成3对共价键,O形成2对共价键,Cl形成1对共价键,即电子式为:![]() ,其结构式为O=N-Cl,
,其结构式为O=N-Cl,
故答案为:坩埚;O=N-Cl;
(2)虚线方框内的操作主要是除去Fe(OH)3,[Pd(NH3)2]2+在盐酸中能以[Pd(NH3)2]Cl2 黄色晶体的形式析出,是否进行虚线方框内的操作,对提高钯的回收率至关重要,其主要原因是Fe(OH)3 为胶状沉淀,对[Pd(NH3)2]2+具有很强的吸附作用,若不进行此操作, [Pd(NH3)2]2+的吸附损失大。
故答案为:Fe(OH)3 为胶状沉淀,对[Pd(NH3)2]2+具有很强的吸附作用,若不进行此操作, [Pd(NH3)2]2+的吸附损失大;
(3)脱氨将Pd(NH3)2Cl2变化为PdCl2,发生反应的化学方程式为Pd(NH3)2Cl2═PdCl2+2NH3↑,最后焙烧之前若不烘干,PdCl2水解生成Pd(OH)2,受热分解,所得产品中会混有 PdO杂质。
故答案为: PdO;
(4)可用“化学放大”法测定样品中的微量 Fe3+:在酸性介质中加入过量的 KI 发生的反应为:2Fe3++2I-=2Fe2++I2,后用CCl4萃取,分去水相后,用肼(N2H4)的水溶液进行还原并反萃取,还原过程中有无污染的气体生成,反应为N2H4+2I2=4I-+N2+4H+。再用过量的 Br2 将反萃取出的 I- 氧化成 IO3- ,煮沸除 Br2后,加入过量的 KI,发生反应:5I-+IO3-+6H+=3I2+3H2O;酸化后用Na2S2O3 标准液进行滴定,发生反应:2Na2S2O3+I2=Na2S4O6+2NaI。经上述步骤后,有以下关系式:2Fe3+~I2~2I-~2IO3-~6I2,样品含量的测定值放大了6倍,还原过程中发生反应的离子方程式 N2H4+2I2=4I-+N2↑+4H+ ,假定萃取达到平衡时,样品在水和萃取剂中的总浓度比为 1∶80,50mL 的水溶液样品,设浓度为c,用 10mL 萃取剂萃取,萃取后溶液中残留的样品浓度为b,萃取剂中的浓度为![]() ,则有
,则有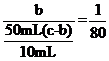 ,
,![]() 萃取后溶液中残留的样品浓度为原溶液的
萃取后溶液中残留的样品浓度为原溶液的![]() 倍(用分数表示)。完成萃取和反萃取操作,在分液漏斗中进行,必须选用的仪器有B(填标号)。
倍(用分数表示)。完成萃取和反萃取操作,在分液漏斗中进行,必须选用的仪器有B(填标号)。
故答案为: 6 ; N2H4+2I2=4I-+N2↑+4H+ ;![]() ; B。
; B。

 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L