新型电池的开发与使用在现代社会中已很普遍,一种水煤气燃料电池的能量转化率可达90%以上。下列说法正确的是( )
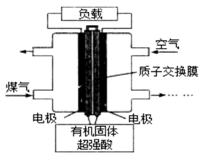
A. 该反应总反应式:CO+H2+O2=CO2+H2O
B. 电路中通过4mol电子,正极消耗112L空气
C. 有机固体中的H+ 在放电时向正极移动,造成正极pH减小
D. 若该电池的能量利用率为90%,则通入10mol水煤气(CO:H2 =1:1),则电路中可产生电子9mol
答案
A
【解析】
【分析】
水煤气燃料电池的负极上通入的是燃料:一氧化碳和氢气,发生失电子的氧化反应,在正极上是氧气发生得电子的还原反应,阳离子移向正极,根据电极反应式确定电子转移的数目并进行计算即可。
【详解】A.一氧化碳和氢气,发生失电子的氧化反应,则水煤气燃料电池发生的总反应式为CO+H2+O2=CO2+H2O,故A正确;
B.电路中通过4 mol电子,正极消耗的是氧气,消耗氧气失1mol,消耗22.4 L×5=112L(标准状况)空气,选项中没有指明气体的状态,故B错误;
C.有机固体中的H+在放电时向正极移动,但是氧气在正极上得电子会消耗氢离子得到水,正极pH增大,故C错误;
D.负极电极反应为:H2-2e-═2H+、CO-2e-+H2O=CO2+2H+,若通入224L即10mol水煤气(CO:H2=1:1),转移电子是20mol,该电池的能量利用率为90%,则电路中可产生电子18mol,故D错误;
故答案为A。
